Photodermatosen – eine interessante Herausforderung für Dermatologen
Im Reigen der Photodermatosen nehmen die idiopathischen Photodermatosen (IPD) eine Sonderstellung ein, da ihre kausale Pathogenese noch nicht vollständig aufgeklärt wurde und sie aufgrund ihrer Epidemiologie und formalen Pathogenese insgesamt ein sehr spannendes Teilkapitel der Photodermatologie darstellen. Aus dem Spektrum der IPD gehe ich in diesem Artikel genauer auf die polymorphe Lichtdermatose, die Hydroa vacciniforme und die solare Urtikaria ein.
Polymorphe Lichtdermatose (PLD)
Die korrekte Bezeichnung für die mit Abstand häufigste idiopathische Photodermatose (IPD) lautet polymorphe Lichtdermatose (PLD) oder polymorphe Lichteruption (PLD). Sie kommt zwar weltweit vor, zeigt aber ein deutliches Nord-Süd-Gefälle mit der höchsten Inzidenz in Skandinavien. Obwohl die PLD auch bei Bevölkerungen mit hohem Hautphototyp zu finden ist, sind vor allem hellhäutige Menschen davon betroffen. Bei Frauen tritt die PLD zwei- bis dreimal so häufig auf wie bei Männern. Darüber hinaus besteht eine gewisse familiäre Disposition.
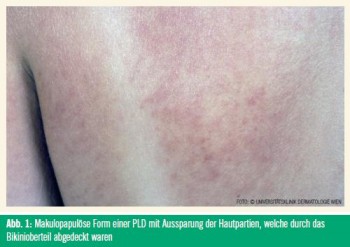
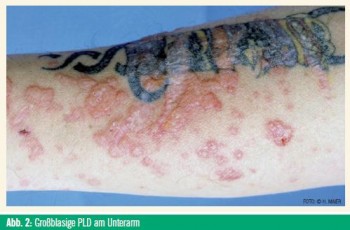
Der klinische Verlauf der PLD ist sehr charakteristisch: Die Patienten berichten, dass es nach zwei bis drei Tagen mit Sonnenexposition an bestimmten Hautarealen zu einem heftig juckenden Hautausschlag kommt, welcher mit jeder weiteren UV-Bestrahlung stärker wird und sich bis zur Unerträglichkeit steigern kann. Die Prädilektionsstellen sind das Dekolletee (Abb. 1), die Streckseiten der Unterarme und der Oberarme, die Streckseiten der Unterschenkel und die Fußrücken, die Ohren und die Retroaurikularregion (bei Kurzhaarfrisur und Sonnenexposition von hinten). Die Effloreszenzen reichen von hellroten Maculae über Papeln und Bläschen/ Blasen (Abb. 2) bis zu follikulär angeordneten Pusteln.
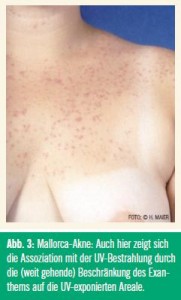
Das Erscheinungsbild variiert von Patient zu Patient – daher kommt die Bezeichnung „polymorph“ –, kann sich aber auch beim einzelnen Patienten im Laufe des Bestehens der Erkrankung wandeln. Zumindest zu Beginn ist die PLD streng auf die UV-exponierten Areale beschränkt. Die meisten Betroffenen entwickeln den ersten Schub zwischen dem 20. und 30. Lebensjahr. Die PLD bleibt dann mehrere Jahrzehnte aktiv und erlischt sehr häufig um das 60. Lebensjahr. Für die Patienten ist das ein schwacher Trost, da das Gros der Sommer-Sonnenurlaube in diesen Lebensabschnitt fällt. Sonderformen sind die Mallorca-Akne (Abb. 3) und die aktinische Purpura (Abb. 4). Bei der Mallorca-Akne treten bei Patienten mit zu Akne neigender Haut bei Anwendung von fettigen Sonnenschutzmitteln an den genannten Prädilektionsstellen follikuläre Pusteln auf.
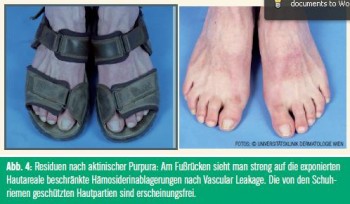
Aufgrund des zur Bestrahlung verzögerten Auftretens der Hauterscheinungen liegt eine Hautreaktion nach dem Muster der Typ-IV-allergischen Reaktion auf ein noch nicht näher definiertes, photoaktiviertes Allergen nahe. Die histopathologischen Untersuchungen läsionaler Haut zeigen ein beträchtliches perivaskuläres Rundzellinfiltrat und damit eine starke vaskuläre Komponente. Diese kommt besonders deutlich bei der so genannten solaren Purpura zum Tragen, bei der es – streng auf die bestrahlten Areale beschränkt – zu petechialen Blutungen kommt.
Die Diagnose: Als wichtigste Differentialdiagnosen gelten chronischer kutaner Lupus erythematodes, toxischirritative/ allergische (Photo-)Kontaktdermatitis und Hydroa vacciniforme. Zum Ausschluss der Differentialdiagnose Lupus erythematodes wird die Bestimmung des Autoantikörpertiters und der Ro- sowie der La-Subsets empfohlen. Im Zweifelsfall ist die Durchführung eines Photoprovokationstests mit einer histopathologischen und immunfluoreszenzoptischen Diagnosesicherung aus den photoprovozierten Läsionen erforderlich. Die routinemäßige Photoprovokationstestung auch bei vollkommen klaren Verhältnissen wurde an den meisten Zentren zu Gunsten einer gezielten Testung bei differentialdiagnostischen Fragestellungen aufgegeben. Der Test ist nur dann valide, wenn die Testbestrahlung in jenen Arealen vorgenommen wird, die auch natürlicherweise von dem Ausschlag betroffen sind.
Die Behandlung des bestehenden Exanthems umfasst neben antipruriginösen Maßnahmen (Kühlsalben, Schüttelmixturen, Antihistaminika) die Verordnung von topischen/systemischen Steroiden sowie die Einhaltung einer konsequenten Sonnenkarenz. Dabei ist der textile Sonnenschutz vor Sonnenschutzmitteln mit sehr hohem UV-Schutz (SPF 50+) zu nennen. Bei UV-Karenz heilt die PLD auch ohne aktive Therapie spontan innerhalb von eineinhalb bis zwei Wochen vollständig und narbenfrei ab.
Prophylaktische Behandlung: Im Zusammenhang mit der PLD ist die prophylaktische Therapie von großer Bedeutung, soll sie doch ein ungestörtes Urlaubsvergnügen gewährleisten. Als effizienteste und zugleich eleganteste Methode gilt das so genannte Photo-Hardening. Darunter versteht man die vorbeugende UV-B-Schmalband-Monophototherapie, die Hochdosis-UV-A1-Monophototherapie sowie die Photochemo – therapie mit Oxsoralen und Breitband-UV-A (8-MOP PUVA).1 12–15 Bestrahlungen, beginnend mit signifikant suberythematogenen Dosen im Spätwinter bis Frühjahr, gewährleisten Erscheinungsfreiheit während der gesamten Sommer- und Herbstsaison. Wichtig ist das sehr langsame Steigern der Dosis im Laufe der Therapie, bei dem sich der behandelnde Arzt einfühlsam an den Angaben des Patienten über eventuelle Symptome orientieren muss.
Alle anderen Methoden wie Chloroquin oder Hydroxychloroquin sind von untergeordneter Bedeutung und studienmäßig schlecht abgesichert. Das viel gepriesene Betacarotin ist bei der PLD – im Unterschied zur erythropoetischen Protoporphyrie – vollkommen nutzlos. Unter den Antioxidanzien spielt lediglich der Extrakt aus dem mittelamerikanischen Farn Polypodium leucotomos eine gewisse Rolle. Die intramuskuläre Gabe eines Depotsteroids vor Urlaubsantritt halte ich persönlich für eine „Verzweiflungstat“. Aber auch für alle anderen Therapieoptionen muss eine nüchterne Nutzen-Schaden-Abwägung stattfinden und eine entsprechende Aufklärung des Patienten erfolgen.
Hydroa vacciniforme
Hydroa vacciniforme (Hydroa aestivale) (HV) ist eine sehr seltene, durch UV-AStrahlung ausgelöste IPD, welche durch ihre mögliche Assoziation mit einer Epstein-Barr-Virus (EBV-)Infektion in den vergangenen Jahren verstärktes wissenschaftliches Interesse hervorgerufen hat. Auch die Differentialdiagnose eines HVähnlichen Lymphoms hat die Aufmerksamkeit auf diese IPD gelenkt.
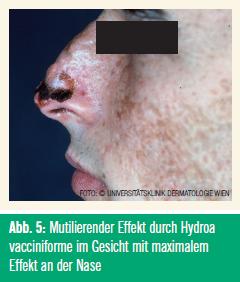
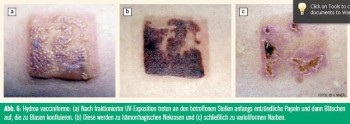
Verlauf: Die Erkrankung tritt weltweit auf, beginnt bereits in der Kindheit und sistiert in der Regel in der Lebensmitte. Der Krankheitsverlauf entspricht weitgehend dem Krankheitsverlauf der PLD. Allerdings gibt es einige wichtige Unterschiede: Anders als bei der PLD ist das Gesicht (Maximum: Nase, Ohren) mitbetroffen (Abb. 5). Nach fraktionierter UV-Exposition treten an den betroffenen Stellen anfangs entzündliche Papeln und dann Bläschen auf, die zu Blasen konfluieren. Diese werden zu hämorrhagischen Nekrosen und schließlich zu varioliformen Narben (Abb. 6). Daher hat die Erkrankung auch ihren Namen. Die subjektiven Symptome werden von den Patienten als lokal brennende Schmerzen angegeben, manchmal geht die Erkrankung auch mit Systemzeichen wie Fieber, Kopfschmerzen und Krankheitsgefühl einher.
Die Diagnosestellung erfolgt in der Regel durch Klinik und Anamnese sowie durch den Ausschluss möglicher Differentialdiagnosen: Histopathologie, Immunfluoreszenzanalytik, Porphyrine im Harn qualitativ und quantitativ, UV-A-Photoprovokationstest. Die Palette der möglichen Differentialdiagnosen ist deshalb so umfangreich, weil sie sehr stark vom Stadium der HV abhängt: papulöses Stadium (PLD, CCLE); Bläschenstadium (PLD, Varizellen, Herpes); Blasenstadium (PLD, Porphyrien, Pseudo-Porphyrien, autoimmunbullöse Dermatosen); Nekrosestadium (Herpes-Virus-Infektionen, Pox- und Parapox-Virus-Infektionen).
Therapie und Prophylaxe: Bei Auftreten der akuten Krankheitserscheinungen steht eine symptomatische Therapiestrategie im Vordergrund (s. PLD). Wie bei PLD konnte gezeigt werden, dass eine prophylaktische PUVA-Therapie zusammen mit UV-Karenz sehr effektiv ist, um neuerliche Schübe zu unterbinden.
Solare Urtikaria
Die dritte IPD, die ich in diesem Artikel vorstelle, ist die solare Urtikaria (SU). Auch sie tritt weltweit auf, (wahrscheinlich) häufiger bei Frauen als bei Männern. Sie zählt ebenfalls zu den seltenen Photodermatosen, ist aber deutlich häufiger als die HV. Die SU wird zu den physikalischen Urtikaria-Formen gerechnet und kann durch optische Strahlung unterschiedlicher Wellenlänge hervorgerufen werden. Neben der UVStrahlung ist sichtbare Strahlung ein häufiger Auslöser.
Verlauf: 15–30 Minuten nach der Lichtexposition kommt es in den bestrahlten Haut arealen zu einem heftig juckenden bis brennenden urtikariellen Exanthem. Sehr, sehr selten erfolgt die Hautreaktion um mehrere Stunden zeitversetzt zur Lichtexposition. In einigen Fällen tritt nur Juckreiz oder ein flaues Erythem auf. Im Unterschied zu PLD und HV, bei denen nur bestimmte Prädilektionsstellen betroffen sind, können die lichtinduzierten Quaddeln bei der SU am gesamten Integument auftreten. In Arealen, die ständig der Sonnenbestrahlung ausgesetzt sind – also eine Art natürliches Hardening aufweisen –, fällt die Reaktion schwächer aus als in unbestrahlten Hautarealen. Erst kürzlich wurde eine fixe solare Urtikaria beschrieben, bei der die Hautreaktionen nur an bestimmten Prädilektionsstellen auftreten.
Wie bei allen anderen Urtikaria-Typen sind die Hauteffloreszenzen auch bei der SU flüchtig und heilen erscheinungsfrei ab. Die SU kann insofern weiter reichende Folgen auf die allgemeine Gesundheit der betroffenen Patienten haben als jede andere IPD, da bei einer generalisierten Urtikaria Schwindelgefühl und Blutdruckabfall bis hin zum Schock als Folge der Flüssigkeitsumverteilung auftreten können. In vielen Fällen ist die SU eine vorübergehende Episode im Leben der Betroffenen und verschwindet nach einigen Jahren wieder.
Als zu Grunde liegenden Mechanismus nimmt man eine Typ-I-Photoallergie an, bei der nicht näher bekannte, im Serum enthaltene Makromoleküle in Mastzelldestabilisierende Allergene umgewandelt werden. Dafür spricht die in den 1950er-Jahren nachgewiesene Transferierbarkeit der urtikariellen Photoreaktivität auf nicht-betroffene Personen durch intrakutane Injektionen des Serums, das von Betroffenen gewonnen wurde.
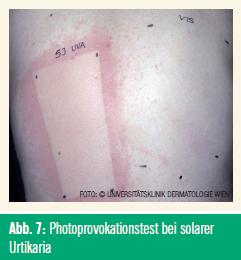
Diagnose und Therapie: Die Diagnose erfolgt mittels Photoprovokationstest im UV-B-, UV-A- und im sichtbaren Bereich der optischen Strahlung (Abb. 7). Mögliche Differentialdiagnosen sind alle anderen Urtikaria-Formen. Bei schweren Reaktionen sind kreislaufunterstützende Maßnahmen erforderlich.
Zur Prophylaxe kommen systemische Antihistaminika, Cyclosporin A und Photo-Hardening (UV-B-Narrow-Band-Monophototherapie, PUVA) zum Einsatz. Sonnenschutzmittel haben nur bei UVinduzierten Formen der SU Erfolg, nicht aber bei SU, welche durch sichtbare Strahlung ausgelöst werden. Für die Photo-Hardening-Prophylaxe von Patienten mit generalisierter SU benötigt man sehr viel Fingerspitzengefühl. Sie gehört daher unbedingt in die Hand von sehr erfahrenen Photodermatologen.
Die IPD sind sehr interessante Intoleranzreaktionen der Haut auf optische Strahlung. Die Kenntnis ihrer klinischen Erscheinungsformen ist der wesentliche Schritt zur Diagnostik und richtigen (prophylaktischen) Therapie. Dadurch erleichtert man den Betroffenen das Leben ungemein und gewinnt treue und zufriedene Patienten. Im Fall von IPD-Patienten, die einer Tätigkeit im Freien nachgehen, ermöglicht ein korrektes ärztliches Vorgehen vielfach den Verbleib im erlernten Beruf oder zumindest die frühzeitige Initiierung eines Umschulungsprozesses.