Die COPD ist nach wie vor als Erkrankung, die durch inhalative Schadstoffe verursacht wird, definiert. Neben dem Hauptrisikofaktor Rauchen spielt die Häufigkeit von Atemwegsinfektionen, vor allem in der Kindheit, eine wesentliche Rolle, erklärt der Experte Prim. Priv.-Doz. Dr. Arschang Valipour. „Die COPD ist keine Erkrankung, die ausschließlich ab dem 40. Lebensjahr beginnt, sondern es bestehen auch gewisse (genetische) Prädispositionen, bevor sich eine COPD als solche manifestiert. Bereits pränatal haben Ernährung, Infektionen und Rauchexposition in der Schwangerschaft einen Einfluss, sogar präkonzeptionell kann das Rauchverhalten der Eltern von Bedeutung sein“, so Valipour.
Aktuelle Daten aus der österreichischen LEAD-Studie1 belegen, dass in Österreich etwa 6 % der Menschen von einer COPD betroffen sind, Männer etwas häufiger als Frauen. Mit steigendem Alter erhöht sich auch die Prävalenz.
„Die Biologika-Therapie wird für die spezielle Kohorte der Patient:innen, die unter Maximaltherapie trotzdem exazerbieren (und erhöhte EOS und/oder FeNO) aufweisen, der nächste Gamechanger; hier mehren sich von Jahr zu Jahr die Studiendaten.“
Diagnostik
Präsentiert sich ein:e Patient:in mit Belastungsdyspnoe und/oder chronischem Husten und/oder Auswurf, ist eine COPD zu vermuten. Neben der Expositionsanamnese und einem Thoraxröntgen, um andere Erkrankungen auszuschließen, ist die Messung der Lungenfunktion (Spirometrie) ein zentrales Element der Diagnostik. Ein Tiffeneau-Index, das Verhältnis von FEV1 (Forced expiratory Volume, das Luftvolumen in der ersten Sekunde eines maximalen, forcierten Ausatmens) zu FVC (Forced vital Capacity, das Gesamtvolumen, das eine Person nach maximaler Einatmung maximal ausatmen kann) < 70 % ist pathognomonisch für die Diagnose einer Atemflussobstruktion. Und hier ist es entscheidend, dass es sich um den postbronchodilatatorischen Wert handelt, also nach der Gabe von einem Bronchodilatator, 15 bis 20 Minuten danach gemessen, wenn eine fixierte Atemflussobstruktion besteht, dann spricht man von einer COPD.
Im Gegensatz zu den GOLD-Kriterien2 berücksichtigen die deutsch-österreichischen Leitlinien3 beim Tiffeneau-Index auch die altersbezogenen Normwerte, da dieser Wert von 70% im Laufe des Lebens nicht gleich bleibt, erläutert Valipour. Darüber hinaus können auch die Ganzkörperplethysmografie („große Lungenfunktion“) sowie die Kohlenmonoxid-Diffusionskapazität (DLCO) zur Diagnose herangezogen werden3, selbst wenn der Tiffeneau-Index als solches nicht pathologisch ist, fasst der Experte zusammen. Auch die Computertomografie wird zunehmend angewendet und dient zur Beurteilung von Komorbiditäten, zur Bestimmung des Phänotyps sowie zur Einschätzung der Prognose.
COPD wird spät diagnostiziert
Der Großteil der Patient:innen wird im GOLD-Stadium II diagnostiziert, hier ist eine Lungenfunktion zwischen 50 % und 80 % vorhanden. Rund 30 % erhalten erst in Stadium III oder IV die Diagnose, d.h., zum Zeitpunkt der Diagnose ist bereits still und leise viel Lungenfunktion verloren gegangen, betont Valipour. Lediglich knappe 20 % werden im Frühstadium (GOLD I) diagnostiziert.4
In einer Beobachtungsstudie aus dem Vereinigten Königreich5 konnte gezeigt werden, dass rund 85 % der Betroffenen, bei denen eine COPD diagnostiziert wurde, in den 5 Jahren vor der Diagnose – eigentlich mit sehr typischen Beschwerden – bereits ärztliche Hilfe gesucht haben, die COPD dennoch nicht diagnostiziert wurde. Erschreckend ist, dass 40 % sogar die Therapie einer Exazerbation erhalten (systemisches Kortison bzw. Antibiotika) haben, es wurde aber trotzdem keine weitere COPD-Diagnostik veranlasst, bedauert der Experte.
Die GOLD-Gruppen
Die Einteilung der Patient:innen in die GOLD-Gruppen2 ist wichtig zur Beurteilung der Symptome und zur Einschätzung des Therapiebedarfes. Hier gab es in den letzten 3 Jahren eine Änderung: Patient:innen werden nun in die Gruppen A, B und E eingestuft (anstelle von A,B,C,D). In die Gruppe A (kaum Symptome und keine Exazerbationen) fallen nicht einmal 5 % der gesamten COPD-Kohorte. In der Gruppe B finden wir Patient:innen mit Symptomen, aber ohne gehäufte Exazerbationen. Haben Betroffene mindestens 2 moderate oder 1 spitalsaufenthaltsbezogene Exazerbation, handelt es sich um Gruppe E. Unter moderat versteht man akute Bronchospasmen und/oder einen Infekt, der systemisches Kortison und/oder Antibiotikum nötig macht. Diese Einteilung ist jetzt unabhängig von FEV1: Dieser Wert kann durchaus hoch sein, man ist aber trotzdem in der Gruppe E. Sie können aber auch einen niedrigen FEV1 haben und in die Gruppe GOLD-B fallen, wenn Sie keine Exazerbationen aufweisen. Eine große Kohortenstudie aus Zentral- und Osteuropa6, 7 zeigte, dass etwa 2 Drittel der stabil betreuten Patient:innen keine gehäuften Exazerbationen haben, während rund 20% bis 30 % in die Kategorie der „exacerbaters“ hineinfallen. Diese Patient:innen haben eine hohe Krankheitsaktivität, und deren Zustand kann sich rasch verschlechtern, sie benötigen daher eine besonders intensive Betreuung, weiß Valipour. Darüber hinaus neigen sie dazu, sich häufig aufgrund der Erkrankung zurückzuziehen, was zu einer geringeren Leistungsfähigkeit und zu einer erhöhten Anfälligkeit für Depressionen führt – ein klassischer Teufelskreis, der auch mit einem erhöhten Risiko für Morbidität und Mortalität einhergeht. Beispielsweise ist in den ersten 30 Tagen nach einer Exazerbation das Risiko für kardiovaskuläre Ereignisse erhöht.
Komorbiditäten auch behandeln
Mindestens 2 Drittel der Patient:innen mit COPD weisen Komorbiditäten wie Hypertonie, koronare Herzerkrankung (KHK), Herzinsuffizienz, Vorhofflimmern oder PAVK auf.8 Begleiterkrankungen spielen eine große Rolle und müssen bei der Therapie berücksichtigt werden: Hier sagen die GOLD-Leitlinien2 ganz klar, die Komorbiditäten sind so zu behandeln, als wenn es die COPD nicht gäbe. Wenn beispielsweise die Indikation für einen Betablocker (KHK oder Herzinsuffizienz) gegeben ist, ist die COPD keine Kontraindikation, betont Valipour.
Therapie der COPD
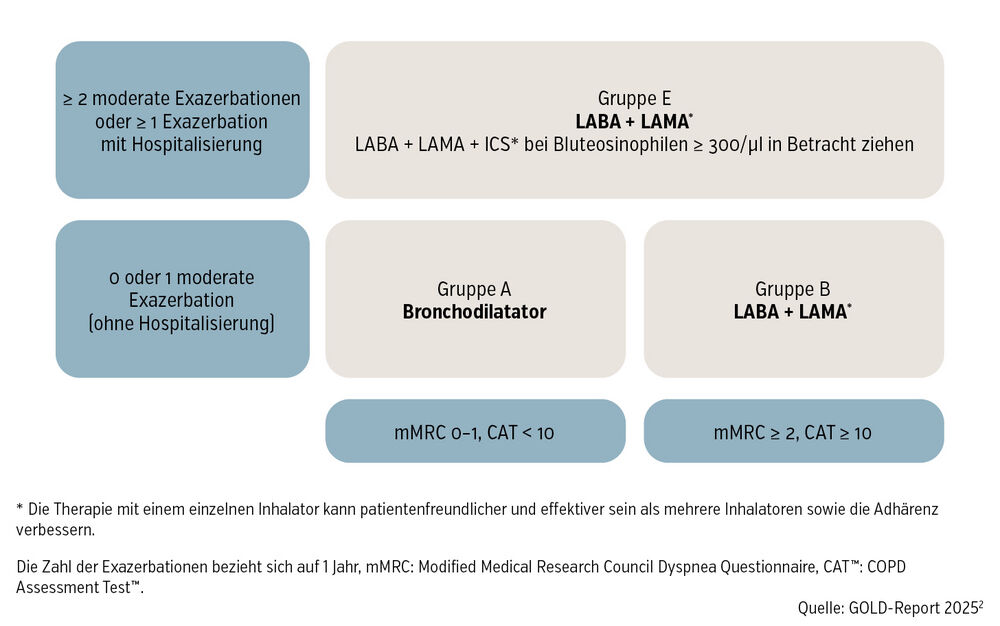
Die Erstlinientherapie (Abb.) basiert auf der Einteilung in die GOLD-Patientengruppen.2 Während Gruppe A, zu der nur ein ganz kleiner Teil der Patient:innen gehört, lediglich einen Bronchodilatator benötigt, ist für Gruppe B ein langwirksamer Muskarinantagonist (LAMA) + langwirksamer Beta-2-Agonist (LABA) indiziert. In der Gruppe E ist die Einstiegstherapie gleich wie für Gruppe B, bei einer Eosinophilie sollte jedoch eine Tripletherapie LAMA+LABA+ICS (inhalatives Kortikosteroid) erwogen werden. Die Basistherapie ist somit in der Regel eine kortisonfreie, obwohl nach wie vor ein beträchtlicher Teil von Patient:innen mit COPD ein LABA+ICS, also eine klassische Asthmatherapie, verordnet bekommt.
Kommt es unter inhalativer Maximaltherapie (Tripletherapie) trotzdem zu Exazerbationen, sollte eine Phänotypisierung erfolgen. Den GOLD-Leitlinien2 entsprechend gibt es 3 Behandlungspfade, wie Valipour veranschaulicht: Roflumilast (bei chronischer Bronchitis), Azithromycin (bei chronischer Bronchitis, Bronchiektasien [Kontraindikation für ICS]) sowie Biologika, hier allen voran Dupilumab (Eosinophile und/oder exhaliertes Stickstoffmonoxid erhöht). Eine große gepaarte Phase-III-Studie9, 10 konnte nachweisen, dass durch die Zugabe von Dupilumab, einem Anti-IL-4/IL-13-Inhibitor, die Exazerbationsrate signifikant gesenkt und die Lungenfunktion verbessert werden konnte. Ähnliche Ergebnisse wurden rezent auch für Mepolizumab, einen Anti-IL-5-Inhibitor, veröffentlicht.11
Nichtmedikamentöse Maßnahmen
Als wichtigste nichtmedikamentöse Maßnahme nennt der Experte den Rauchstopp: Es gibt Angebote wie das Rauchfrei Telefon der Gesundheitskassen und des Bundesministeriums oder die Initiative „Don’t smoke“ der Österreichischen Krebshilfe. Die betreuenden Lungenfachärzt:innen haben sehr viel Erfahrung und können die Patient:innen bei der Raucherentwöhnung unterstützen. Sie gelingt meist auch gut im Rahmen einer Rehabilitation, gepaart mit Ausdauertraining und Patientenschulungen, um das Selbstmanagement der Erkrankung zu erlernen. Eine weitere wesentliche Maßnahme ist die Infektionsprävention durch Impfungen (RSV, Herpes Zoster, Pertussis, Pneumokokken, Influenza, COVID-19), durch die Morbidität und Mortalität gesenkt werden können.