Dermatomyositis – State oft the Art und neue Therapiekonzepte
Klinik und Diagnose
An sich ist die Dermatomyositis (DM) eine seltene (Prävalenz: 1 : 100.000), jedoch manchmal dramatisch verlaufende Erkrankung. Der systemische Aspekt dieser Erkrankungen wird durch die Möglichkeit einer Lungen- oder Herzbeteiligung unterstrichen. Die Zielorgane dieser Entzündung sind aber, wie der Name der Erkrankung schon ausdrückt, der Muskel und die Haut. Die DM kann PatientInnen in jedem Lebensalter betreffen. Meist kommt es zu einem schleichenden Beginn. Zu den typischen und auch für die Diagnose wichtigen Hautveränderungen zählen das heliotrope Exanthem, welches im Bereich der Augenlider, im Gesicht generell, im Bereich der Knie, der Ellbogen auftreten kann. Zusätzlich können sich PatientInnen mit typischen Veränderungen im Bereich der Fingerknöchel (Gottronsche Papeln), oder der Handflächen („mechanic hands“) präsentieren. Die Calcinosis cutis findet man eher bei der juvenilen Form der DM. Der Muskelbefall bei der DM ist meist symmetrisch und betrifft hauptsächlich proximale Muskelgruppen (Becken- und Schultergürtel).
Malignomsuche ist unerlässlich: Wichtig zu wissen ist, dass die DM in bis zu 15 % der PatientInnen mit einer malignen Erkrankung assoziiert sein kann. Es handelt sich meist um Adenkarzinome der Cervix, der Lunge, der Ovarien, des Pankreas, des Magens oder der Harnblase. Deshalb ist bei PatientInnen mit neu diagnostizierter DM eine Malignomsuche unerlässlich. Hierzu zählen natürlich eine genaue Anamnese und physikalische Krankenuntersuchung ebenso wie ein altersund geschlechteradaptiertes Tumorscreening (z. B. Bestimmung von PSA, Mammografie, Koloskopie, Thoraxröntgen, Abdomensonografie …). Die Malignome können sowohl gleichzeitig als auch vor oder nach Beginn der DM auftreten. Deshalb wird ein regelmäßiges onkologischen Screening (jährlich) vor allem in den ersten 2 Jahren der Erkrankung empfohlen.
Die differenzialdiagnostische Abgrenzung der DM zu anderen muskulären Erkrankungen ist aufgrund der typischen Hautveränderungen in vielen Fällen erleichtert. Letztendlich erfolgt die Diagnose durch Kombination einer exakten Anamnese, des Muskelbefallstyps, der Bestimmung der Muskelenzyme (Kreatinphosphokinase, Aldolase sowie der GOT, GPT), der Immunologie (in bis zu 80 % der PatientInnen findet man pos. ANA), der Ergebnisse der Elektromyographie (EMG) und der Ergebnisse der Muskelbiopsie. Die Muskelbiopsie sollte in einem betroffenen (entzündeten) Muskel (meist Quadriceps oder Deltoideus) durchgeführt werden. Hinweise hierfür können die klinische Unersuchung oder auch die MRT liefern. Interessanterweise unterscheidet sich die Histologie bei DM, PM und IBM. So findet man bei der DM entzündliche Infiltrate vorwiegend im Bereich von Blutgefäßen, während man bei der PM und IBM diese Infiltrate im Bereich von Muskelfasern beobachtet. Die IBM unterscheidet sich von der DM und PM dadurch, dass man histologisch so genannte „rimmed vacuoles“ findet, die Tubulofilamente enthalten. Weiters findet man bei der IBM Kongorot-positive Amyloidablagerungen.
Therapie der Dermatomyositis
Trotz der Ungewissheit über die Ursachen der DM ist aufgrund der Histologie und des Vorkommens von Autoantikörpern eine autoimmunologische Genese wahrscheinlich. Deshalb sind Kortikosteroide immer noch die Standard- oder First-Line-Therapie dieser Erkrankung. Normalerweise wird mit einer Dosis von ca. 1 mg/kg KG Aprednisolon begonnen. Bei schweren Verläufen kann diese Dosis über einen kurzen Zeitraum (z. B. für 3 Tage) auch auf 1 g/Tag erhöht werden. Diese Therapiekonzepte beruhen jedoch mehr auf Erfahrung als auf evidenzbasierter Medizin, da es generell zur DM kaum randomisierte, kontrollierte, klinische Studien gibt. In den weiteren Wochen bzw. Monaten sollte es dann zu einer schrittweisen, langsamen Reduktion der Kortikoidsteroiddosis kommen. Kann die Kortikosteroiddosis aufgrund einer weiterhin anhaltenden hohen Krankheitsaktivität oder sogar aufgrund eines weiteren Schubs nicht reduziert werden, so kommen andere Therapeutika, wie Azathioprin oder Methotrexat zum Einsatz. Azathioprin wird normalerweise in einer Dosierung von 1,5–2 mg/Tag oral verabreicht. Hierzu ist jedoch anzumerken, dass die volle Wirkung erst nach mehreren Wochen bis Monaten eintritt. Hinsichtlich potenzieller Nebenwirkungen sind regelmäßige Kontrollen der Leberwerte und des Blutbilds empfohlen. Eine weitere Option ist Methotrexat (MTX). MTX wird ebenso oral verabreicht. Die Dosierung liegt bei bis zu 25 mg 1-mal/Woche. Auch bei MTXist die Leber sowie auch das Blutbild engmaschig zu kontrollieren. MTX wird aufgrund einer möglichen Akkumulation bei PatientInnen mit Nierenfunktionsstörungen nicht empfohlen. Ähnlich wie bei Azathioprin setzt die Wirkung von Methotrexat erst nach mehreren Wochen ein. Sollten Azathioprin und auch MTX nicht wirken, werden intravenöse Immunglobuline (IVIG), MabThera oder Mycophenolat Mofetil empfohlen. Hier ist wiederum anzumerken, dass bis auf IVIG keine dieser Therapien in einer randomisierten kontrollierten Studie getestet wurden. Bzgl. IVIG ist der Wirkmechanismus nicht ganz klar. Es dürfte jedoch durch IVIG zu einer Blockade von Fc-Rezeptoren kommen. Dadurch wird die Aufnahme von Immunkomplexen und somit die Aktivierung von Leukozyten gehemmt. Nichtsdestotrotz zeigte eine randomisierte, placebokontrollierte Studie mit 15 DM-PatientInnen ein gutes Ansprechen auf IVIG. In dieser Studie wurden IVIG (2 g/kg Körpergewicht) 1-mal/Monat verabreicht. Bis auf Kopfschmerzen während der Infusion wurden über keine Nebenwirkungen berichtet. Die Therapie mit IVIG ist jedoch äußerst kostenintensiv.
Neues Therapiekonzept: Immunadsorption
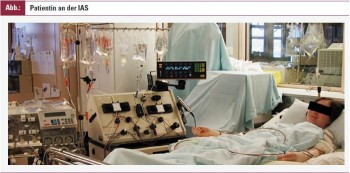
Da die therapeutischen Optionen für DM limitiert, oft nicht adäquat durch Studien untersucht oder schlichtweg nebenwirkungsreich sind, gibt es Grund, neue therapeutische Konzepte zu finden. Eine Therapieoption könnte in der Immunadsorption (IAS) liegen. Die IAS ist ein extrakorporales Therapieverfahren, bei dem pathologische Immunkomplexe und Autoantikörper, wie sie bei der Dermatomyositis vorkommen, entfernt werden. Um Antikörper und Immunkomplexe zu entfernen, wird Plasma der PatientInnen über einen extrakorporalen Adsorber geleitet. In diesem Adsorber befinden sich Substanzen mit hoher Affinität zu Antikörper. Das antikörperdepletierte Plasma wird dem/der PatientIn wieder zurückgeführt. Dies ist ein wichtiger Unterschied zu Plasmapherese/Plasmaaustausch, bei dem das entfernte Plasma verworfen wird. Somit können bei IAS deutlich höhere Plasmavolumina behandelt werden. Dies ist deshalb wichtig, weil eine randomisierte, placebokontrollierte Studie zeigte, dass Plasmaaustausch keinen Effekt auf die Krankheitsaktivität der DM oder PM hatte. Anzumerken ist auch, dass die IAS bisher erfolgreich auch bei anderen Autoimmunerkrankungen wie z. B. SLE zur Anwendung gekommen ist.
Eigene Erfahrungen: In den letzten 5 Jahren wurden an der Klinik für Innere Medizin III fünf PatientInnen (2 Frauen, 3 Männer) mit aktiver Dermatomyositis trotz Therapie mit Aprednislon als Monotherapie oder in Kombination mit Methotrexat oder Azathioprin behandelt. Nach nur einem Monat IAS-Therapie kam es zu einer Verbesserung in allen PatientInnen. Insgesamt wurde die Therapie mit Immunadsorption von allen PatientInnen gut toleriert, und es kam zu keinen nennenswerten Nebenwirkungen, sodass nun eine größere, kontrollierte Studie geplant ist.