Bisphosphonat als adjuvante Therapie des Mammakarzinoms – AZURE-Studie
Mit dieser Zielsetzung wurden 3.360 Brustkrebspatientinnen in den Jahren 2003–2006 randomisiert und entweder mit Chemotherapie oder Chemotherapie + Zoledronsäure (4 mg, halbjährlich über 5 Jahre) behandelt. Das Kollektiv bestand aus Hochrisikopatientinnen mit invasivem Mammakarzinom in den Stadien II/III, T3/4 oder Lymphknotenbeteiligung. Etwa 80 % der Patientinnen waren östrogenrezeptorpositiv. Primärer Studienendpunkt war das krankheitsfreie Überleben (DFS) nach 3 Jahren (DFS definiert als Brustwandre – zidiv, regionales Rezidiv, Auftreten von Fernmetastasen und Tod ohne Rezidiv).
Ergebnisse: Nach einem Follow-up von 5 Jahren konnte der primäre Studienendpunkt in der Gesamtauswertung aller Patientinnen nicht verbessert werden. Lokoregionale Rezidive, Fernmetastasen, ipsilaterale oder kontralaterale Mammakarzinomen traten in beiden Gruppen in gleicher Verteilung auf.
Ergebnisse nach Menopausenstatus: Entscheidende Unterschiede ergaben sich in Abhängigkeit vom Menopausenstatus.
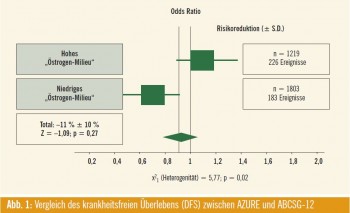
- Bei prämenopausalen Patientinnen mit intaktem Östrogenhaushalt („high oestrogen environment“) wurde in der AZURE-Studie keine Verbesserung des krankheitsfreien Überlebens erzielt: Zum Vergleich: In der ABCSGStudie 12 konnte Zoledronsäure bei prämenopausalen Patientinnen, die endokrin behandelt wurden („low oestrogen evironment“) das krankheitsfreie Überleben um 36 % verbessern: Es wurden sowohl kontralaterale wie auch lokoregionale Rezidive und Fernmetastasen verringert2 (Abb. 1).
- Bei etablierter Postmenopause (physiologisches „low oestrogen evironment“) konnte die Gabe von Zoledronsäure in der AZURE-Studie nicht nur das krankheitsfreie Überleben um 24 % signifikant verbessern, sondern auch das Mortalitätsrisiko um 29 % signifikant verringern (p = 0,017) (Abb. 1).
Schlussfolgerung der Autoren: Quer durch das Kollektiv chemotherapeutisch behandelter Patientinnen mit Mammakarzinom in den Stadien II/III konnte der adjuvante Einsatz von Zoledronsäure das Gesamtergebnis nicht beeinflussen. Vordefinierte Subgruppenauswertungen zeigten jedoch eine signifikante Abweichung in Ab – hängigkeit vom Menopausenstatus mit einem Überlebensvorteil für postmenopausale Patientinnen. Die Autoren hielten fest, dass der Erfolg einer adjuvanten Bisphosphonat-Therapie offenbar an niedrige Östrogenspiegel gekoppelt ist.
1 Adjuvant Treatment with Zoledronic Acid in Stage II/III Breast Cancer. The AZURE Trial (BIG 01/04). Coleman RE et al., SABCS 2010, Abstract #S4–5
2 Endocrine Therapy plus Zoledronic Acid in Premenopausal Breast Cancer, Michael Gnant et al., N Engl J Med 2009; 360:679–691
INTERWIEW
Schlagende Unterschiede, gemeinsame Endstrecke
„Insgesamt betrachtet konnte die Bis – phosphonat-Therapie in der AZURE-Studie bei einem breiten Patientenkollektiv keinen Vorteil erzielen, was sicher enttäuschend ist. Dennoch weisen Auswertungen zum Menopausenstatus auf signifikante Unterschiede hin, die in vieler Hinsicht interessant sind. Was prämenopausale Patientinnen betrifft, stehen die Ergebnisse der AZURE-Studie zunächst im diametralen Gegensatz zu den Ergebnissen der ABCSG-Studie 12. In beiden Studien war die Fallzahl repräsentativ, die Ergebnisse können also kein Zufall sein, allerdings hat sich das Kollektiv der beiden Studien dadurch unterschieden, dass in AZURE keine Patientin eine ovarielle Suppression erhalten hat – praktisch alle Patientinnen waren chemotherapiert –, während unsere Patientinnen keine Chemotherapie erhalten haben, sondern eine endokrine Therapie und Goserelin als ovarielle Suppression. Quer durch sämtliche klassische Subgruppen hinweg (z.B. Lymphknotenstatus, Grading, Tumorgröße) zeigt das letzte Update der ABCSGStudie 12, dass die Wirkung von Zoledronsäure gleichmäßig verteilt war. Nur bei sehr jungen Patientinnen mit immer noch verbleibender ovarieller Restfunktion war die Wirkung weniger ausgeprägt: Würde man diese Patientinnen aus der Gesamtauswertung herausfiltern, wären die Ergebnisse sogar noch deutlicher. In der AZURE-Studie war die Wirkung bei Patientinnen in der Postmenopause mit einer Reduktion des Mortalitätsrisikos um knapp 30 % am stärksten. Wenn solche Ergebnisse keinerlei Berücksichtigung mehr finden sollten, wäre das in Wahrheit ein Dilemma. Das entscheidende Kriterium, in dem sich beide Studien mit positiven Daten überschneiden, dürfte der Östrogenhaushalt sein: Patientinnen unserer Studie waren ovariell supprimiert, wurden damit in den Menopausenstatus versetzt (mit Ausnahme einer gewissen östrogenen Restfunktion bei ganz jungen Patientinnen) und waren auf diese Weise in einer ähnlichen Situation wie deutlich postmenopausale Patientinnen in AZURE. Unter diesem Aspekt sind die Ergebnisse beider Studien letztlich wieder kongruent. Dort, wo kein Östrogen mehr vorhanden ist, kommt das Bisphosphonat als adjuvante Therapie zur Wirkung. Mit anderen Worten: Wenn man Mikrometastasen im dormierenden Zustand halten möchte, dann darf man nicht nur den Knochen als Target sehen und den Knochenstoffwechsel mit dem Bisphosphonat herabsetzen, sondern muss auch noch das Östrogen als starken Wachstumsstimulus unterdrücken, was in meinen Augen plausibel ist und eine sehr gute Erklärung bietet. In der AZURE-Studie besteht zwischen prä- und postmenopausalen Patientinnen eine derart ausgeprägte Heterogenität, wie man sie in Subgruppenauswertungen sonst nicht findet – oder nur dann, wenn wirklich unerwartete Ereignisse eintreffen; sodass wir aktuell mit folgender Situation konfrontiert sind: mit einem negativen Ergebnis quer über alle Patientinnen und einem deutlich positiven Ergebnis an über 1100 postmenopausalen Patientinnen, bei denen Zoledronsäure eine Senkung der Mortalität um fast 30 % erreichen konnte. Bei östrogensupprimierten prämenopausalen Patientinnen der ABCSG-Studie 12 sind die Ergebnisse ebenfalls signifikant, und zwar in einer Größenordnung, wie man sie im adjuvanten Setting nur mit den besten Therapien erreicht. Das heißt, wir verfügen über eine hohe klinische Evidenz mit einer wirklich nennenswerten Mortalitätsreduktion durch eine kostengünstige Therapie, die nahezu nebenwirkungsfrei verabreicht werden kann, und dennoch ist es fraglich, ob dieser Benefit den Patientinnen auch zukommen kann. Es besteht aber die Hoffnung, dass das Bisphosphonat bei gleichzeitig östrogensupprimierten Patientinnen doch noch eine Indikation findet.“