Impfungen bei onkologischen Patienten
Die richtige Anwendung von Impfungen bei Patienten mit onkologischer bzw. hämato-onkologischer Grunderkrankung kann aufgrund der unterschiedlich schwerwiegenden Immunsuppression durch die zugrunde liegende Erkrankung sowie der Vielfalt an antineoplastischen Therapien herausfordernd erscheinen. Von einer schweren Immunsuppression muss man u. a. bei Patienten mit metastasierter Neoplasie, mit einer akuten hämatologischen Erkrankung, bei Therapie mit monoklonalen Antikörpern wie Rituximab, bei Zustand nach Stammzelltransplantation (für mind. 2 Jahre) oder rezent stattgefundener Radiatio ausgehen. Klassische Chemotherapien mit zytoreduktiven Substanzen üben einen myelosuppressiven Effekt mit daraus resultierender Panzytopenie aus. Die Effektivität von Impfstoffen kann dadurch reduziert sein, jedoch ist die Wirkung der Chemotherapeutika auf das Immunsystem sehr unterschiedlich.
Trotz der facettenreichen Therapien können auf Basis von aktuellen Guidelines1, 2 einige (beinahe) allgemeingültige Prinzipien zum Vorgehen beim Impfen des onkologischen Patienten festgelegt werden.
Totimpfstoffe auch während laufender Chemotherapie möglich
Die Sorge, dass Impfungen während einer Chemotherapie grundsätzlich nicht wirksam oder vielleicht für den Patienten schädlich sind, ist bei Totimpfstoffen unbegründet. Die Frage nach dem optimalen Timing in Zusammenhang mit einer laufenden Chemotherapie ist nicht ganz sicher zu beantworten. Bei zytoreduktiven Therapien sollte man die Phase der Panzytopenie zum Impfen vermeiden, d. h., zu Beginn des Zyklus impfen. Eine Kontrolle der Impfantwort mittels Titer ist bei speziellen Situationen (siehe unten) in Erwägung zu ziehen.
Lebendimpfstoffe sind bei Immunsuppression kontraindiziert
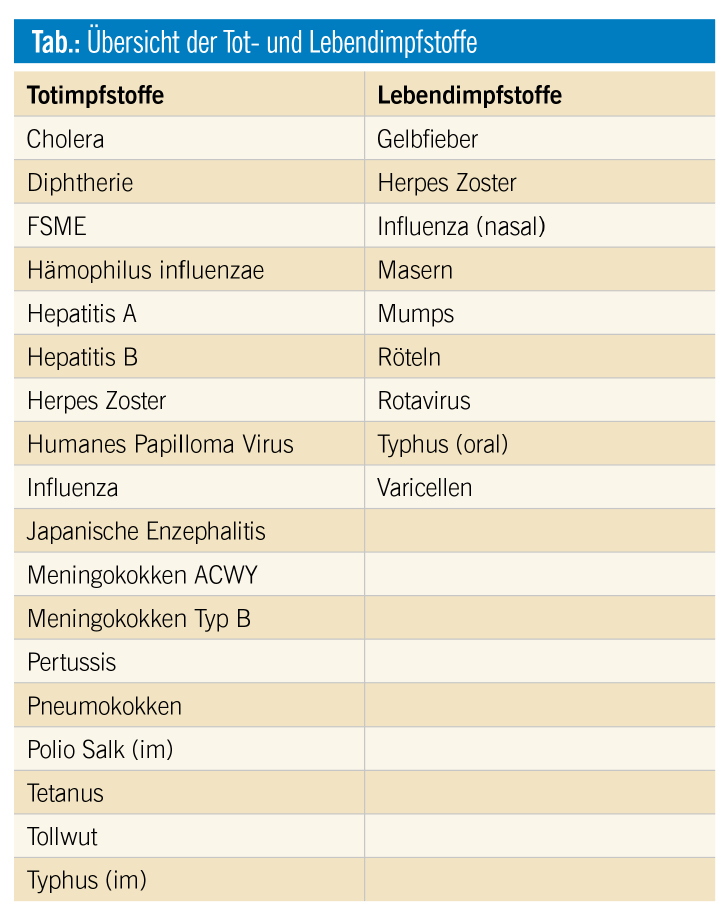
Anders als bei Totimpfstoffen ist von einer Impfung mit Lebendimpfstoffen bei schwerer Immunsuppression oder laufender Chemotherapie immer abzusehen. Insgesamt betrifft das aber nicht viele Impfstoffe (Tab.), relevant dürfte hier die Mumps-Masern-Röteln-Impfung sein, v. a. angesichts der rezenten Zunahme von Masernfällen in der Bevölkerung. Es würde sich daher empfehlen, den Impfstatus schon vor Beginn einer Chemotherapie zu klären. Bei negativem Serostatus darf bis spätestens vier Wochen vor Beginn einer Therapie geimpft werden. Ansonsten können Lebendimpfstoffe frühestens sechs Monate nach Abschluss der Chemotherapie verabreicht werden; bei monoklonalen Antikörpern wie Rituximab frühestens nach 12 Monaten.
Bis vor kurzem war nur eine Lebendimpfung gegen Herpes Zoster möglich, nun steht auch ein inaktivierter Impfstoff zur Verfügung (Shingrix®), welcher sich in Studien mit onkologischen Patienten als wirksam und sicher erwiesen hat und auch während laufender Chemotherapie geimpft werden kann.3 Angesichts dessen, dass Herpes Zoster häufig im Rahmen einer Immunsuppression auftritt, ist die Möglichkeit einer Impfung in diesem Kontext ein bedeutsamer Fortschritt.
Besonders wichtig: Influenza und Pneumokokken
Zur Reduktion der Morbidität und Mortalität ist eine Impfung gegen Influenza und Pneumokokken von größter Bedeutung. Die Impfung gegen Influenza sollte vor Beginn der Grippesaison jährlich stattfinden. Es gibt Daten, welche eine zweimalige Impfung pro Saison v. a. bei Patienten mit hämato-onkologischen Erkrankungen nahelegen4, allerdings bestehen diesbezüglich bis jetzt keine klaren Empfehlungen. Die Verwendung des adjuvierten Influenza-Impfstoffes (FLUAD®), welcher für Personen über 65 Jahre entwickelt wurde, ist auch bei Patienten mit einem geschwächten Immunsystem sinnvoll. Eine Studie bei Patientinnen mit Brustkrebs hatte eine bessere Wirksamkeit bei Impfung zu Beginn des Chemotherapiezyklus nachgewiesen.5 Laut einer rezenten Studie hat der Zeitpunkt der Influenza-Impfung, also zu Beginn oder während des Chemotherapie-Zyklus, keinen signifikanten Einfluss auf die Seroprotektion.6 Zusammenfassend ist die saisonale Influenza-Impfung für onkologische Patienten wichtig und kann im Grunde auch jederzeit während einer Chemotherapie angewendet werden.
Ebenfalls hervorzuheben ist die Impfung gegen Pneumokokken, hierfür stehen ein 13-valenter Konjugatimpfstoff (Prevenar13®) und ein 23-valenter Polysaccharidimpfstoff (Pneumovax23®) zur Verfügung. Wichtig ist zu beachten, dass Polysaccharidimpfstoffe eine sogenannte „Hyporesponsiveness“ auslösen können. Dies bedeutet, dass bei Verabreichung weiterer Impfstoffe gegen Pneumokokken die Immunantwort schwächer wird. Folglich ist eine Boosterung des Polysaccharidimpfstoffes nicht möglich. Außerdem wird nur durch den Konjugatimpfstoff ein immunologisches Gedächtnis induziert. Daher erscheint es sinnvoll, zuerst den Konjugatimpfstoff und dann in Abstand von mindestens zwei Monaten den Polysaccharidimpfstoff zu verabreichen („prime-and-boost“-Strategie), um eine möglichst effektive und breite Abdeckung gegen die verschiedenen Pneumokokken-Serotypen zu erzielen.
Trotz dieser Prinzipien besteht bei jedem Patienten eine individuell zu beurteilende Situation. Auf einige spezielle Indikationen im Hinblick auf Impfungen soll im Folgenden noch kurz hingewiesen werden.
Impfen bei Asplenie
Patienten mit Asplenie, sei diese postoperativ oder funktionell, müssen unbedingt gegen bekapselte Bakterien geimpft werden. Konkret bedeutet dies, dass gegen Pneumokokken (erst Prevenar®, nach 8 Wochen Pneumovax23®), Meningokokken ACWY (Nimenrix®, Menveo®) und Hämophilus influenzae Typ B (ActHib®) geimpft werden soll. Des Weiteren sind nun auch Impfstoffe gegen Meningokokken Typ B (Bexsero®, Trumenba®) auf dem Markt erschienen. Da es hier noch keine Daten gibt, fehlen konkrete Empfehlungen, jedoch erscheint eine Impfung bei Patienten mit Asplenie sinnvoll.
Impfen bei Immuntherapien
Bekannt ist die Wirkung von Rituximab, welches auf CD20 abzielt und dadurch die B-Zellen depletiert (dies gilt auch für andere CD20-Antikörper, z. B. Ofatumumab). Da die Antikörper-bildenden B-Lymphozyten im Zuge dessen fehlen, ist jegliche Impfung während einer solchen Therapie und für mindestens sechs Monate danach wirkungslos. Patienten, welche Rituximab erhalten haben, können folglich nach frühestens sechs Monaten neuerlich mit Totimpfstoffen geimpft werden. Bei Grundimmunisierung oder Lebendimpfstoffen sollen mindestens 12 Monate Abstand gehalten werden. Um den idealen Zeitpunkt zu bestimmen, kann es hilfreich sein, zuerst eine Lymphozyten-Typisierung durchzuführen. Außerdem sollte zur Beurteilung der Impfantwort vor und nach Impfung eine Titerkontrolle stattfinden. Dies gilt auch für Substanzen wie den Tyrosinkinaseinhibitor Ibrutinib, welche die Signalübertragung über den B-Zell-Rezeptor inhibieren und damit die Impfantwort massiv einschränken.2
Impfen nach autologer und allogener Stammzelltransplantation
Zuletzt seien noch Patienten nach Stammzelltransplantation (HSCT) erwähnt, welche sowohl nach autologer als auch allogener HSCT eine komplette Grundimmunisierung für alle empfohlenen Impfungen benötigen. Für dieses sehr spezielle Patientenkollektiv gibt es eigene umfangreiche Empfehlungen7, welche hier nur kurz angeschnitten werden können. Patienten nach allogener Transplantation (Fremdspender) leiden unter einer mehrfachen Immunsuppression – medikamentös, durch die Graft-versus-Host-Erkrankung (GvHD) sowie die verzögerte Immunrekonstitution, welche für Lymphozyten 1–2 Jahre beträgt. Daher ist der richtige Zeitpunkt, um mit dem Impfen zu starten, vom Ausmaß der Immunsuppression abhängig. Es sollte mit der konjugierten Pneumokokken- sowie je nach Saison mit der Influenza-Impfung 3–6 Monate nach HSCT begonnen werden. Die meisten Patienten können ein Jahr nach HSCT alle gängigen Totimpfstoffe erhalten. Für die jeweiligen Impfschemata gibt es nur begrenzt Daten. Für die meisten Totimpfstoffe gilt, dass diese drei Mal im Abstand
von einem Monat und nach einem Jahr nochmals als Booster verabreicht werden. Bei diesen Patienten kann auch der für Kinder zugelassene 6-fach-Kombinationsimpfstoff (DTaP/Polio/Hib/HepB) verwendet werden, welcher eine höhere Antigen-Dosis für Diphtherie und Pertussis aufweist sowie zusätzlich gegen Hämophilus influenzae immunisiert. Gegen Pneumokokken sollte dreimalig der Konjugatimpfstoff und nach einem Jahr bei fehlender GvHD der Polysaccharidimpfstoff einmalig als Booster eingesetzt werden (bei GvHD nur Konjugatimpfstoff). Lebendimpfstoffe sind frühestens 2 Jahre nach HSCT möglich, wenn die Immunsuppression bereits seit einem Jahr abgesetzt ist und keine GvHD besteht. Bei Patienten nach HSCT empfiehlt es sich, vor Beginn und nach Abschluss der Grundimmunisierung eine Titerkontrolle zur Bestimmung der Impfantwort durchzuführen.
Zusammenfassend können onkologische Patienten mit Totimpfstoffen wirksam immunisiert werden, ausgenommen sind Patienten mit Immuntherapien wie Rituximab. Besondere Wichtigkeit haben die Impfung gegen Influenza und jene gegen Pneumokokken. Zu den Neuheiten zählen der Totimpfstoff gegen Herpes Zoster sowie die Möglichkeit, Patienten mit Asplenie gegen Meningokokken Typ B zu impfen. Bei besonderen Fragestellungen, insbesondere bei Immuntherapien sowie Patienten nach HSCT, empfiehlt es sich, Spezialambulanzen zu konsultieren.