Bethesda-Terminology-System: Zeitgemäße und praxisrelevante Nomenklatur
Die Schilddrüsenzytologie ist eine kosteneffektive und zielsichere diagnostische Abklärungsmethode für Schilddrüsenknoten. Im Vergleich zu anderen klinischen Abklärungsmethoden (z. B. Ultraschalluntersuchung, Szintigrafie …) zeigt die Feinnadelaspirationszytologie (FNA) eine relativ hohe Spezifität und Sensitivität.1, 2
Eine zeitgemäße Schilddrüsenzytologie verlangt eine Klassifikation. Diese bringt zahlreiche Vorteile, insbesondere werden dadurch die pathologischen Befunde für den Kliniker verständlich und vergleichbar. Darüber hinaus können sich diagnostisch-therapeutische Algorithmen ableiten lassen.2
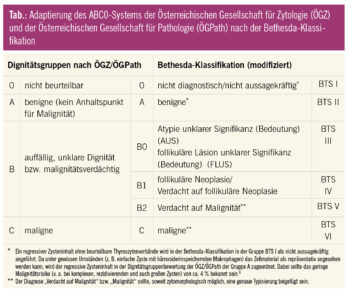
Die Klassifikation der Schilddrüsenzytologie erfolgt in vielen Ländern unterschiedlich3, wobei die Bethesda-Klassifikation (Bethesda-Terminology-System, BTS) der Amerikanischen Gesellschaft für Schilddrüsenerkrankungen (American Thyroid Association, ATA) am häufigsten und auch in vielen europäischen Ländern verwendet wird.2 Dabei wurden viele nationale Klassifikationen, wie z. B. auch in Österreich, in die Bethesda-Klassifikation übersetzt (Tab.).3–5
Die Bethesda-Klassifikation
Die Bethesda-Klassifikation ist ein 6-gradiges System, das ausschließlich für die Schilddrüsenpunktion entworfen wurde und weitgehend evidenzbasiert ist. Der Vorteil in diesem System liegt in der klaren Zuordnung der Malignitätswahrscheinlichkeit in den einzelnen Gruppen. Darüber hinaus erlaubt diese Klassifikation aufgrund ihrer internationalen Verwendung insbesondere in Studien eine internationale Vergleichbarkeit. Es folgt eine kurze Vorstellung der einzelnen Gruppen:
BTS I – nicht diagnostisch/nicht aussagekräftig (Dignitätsgruppe 0 nach ÖGZ und ÖGPath): In dieser Gruppe lässt das Zellbild keine verlässliche Interpretation zu. In der Regel sind in etwa 2–20 % der FNA der Schilddrüse nicht beurteilbar.6 Als Grund findet sich neben der Natur des Knotens (z. B. sklerosierter Knoten) insbesondere bei einem hohen Anteil an BTS-I-Befunden eine fehlerhafte Punktionstechnik. Höhere Anteile an nicht beurteilbaren Biopsien kommen v. a. bei unerfahrenen Punkteuren vor.7
BTS II – benigne (Dignitätsgruppe A nach ÖGZ und ÖGPath): Hierbei handelt es sich um Zellbilder, die keinen Hinweis für Malignität aufweisen. Hier wird eine klinische Kontrolle empfohlen, die Malignitätsrate liegt bei 0–3 %.
BTS III – follikuläre Läsion unklarer Signifikanz/Atypie unklarer Signifikanz (Dignitätsgruppe B0 nach ÖGZ und ÖGPath): Diese neu geschaffene Befundgruppe ist sehr heterogen. Sie umfasst Zellbilder, die weder einer anderen Verdachtsgruppe, noch der benignen Gruppe zugeordnet werden können. Aufgrund der Heterogenität und der hohen Interobserver-Variation ist die Gruppe umstritten.8–10 Häufig sind Einschränkungen der Beurteilbarkeit, wie zum Beispiel Blutüberlagerungen oder geringer Zellgehalt die Ursache für die Verwendung dieser Gruppe, wodurch sich auch die Vorgehensweise der Repunktion rechtfertigt. Die Malignitätsraten sind aber je nach Studie sehr unterschiedlich (von 2 % bis 30 %!).11 Der Pathologe sollte diese Gruppe nur selten (< 7 % der FNA) verwenden; weiters ist hier eine Kommunikation zwischen Pathologe und Kliniker zum weiteren Vorgehen (operative Abklärung oder Repunktion) empfehlenswert.
BTS IV – follikuläre Neoplasie (Dignitätsgruppe B1 nach ÖGZ und ÖGPath): Das Zellbild einer follikulären Neoplasie kann sowohl eine benigne (Adenom, adenomatöse Hyperplasie) als auch eine maligne (follikuläres Karzinom) Läsion sein, da diese Entitäten nur durch histologische Kriterien (Kapseldurchbruch, Kapselgefäßeinbruch) differenziert werden können. Die Malignitätswahrscheinlichkeit liegt laut Literatur bei 15–30 %. Die Malignitätsraten hängen dabei, v. a. bei endemischen Strumagebieten, auch von der klinischen Selektion der punktierten Knoten ab (z. B sind szintigrafisch heiße Knoten praktisch nicht maligne).8 In der Regel stellt die follikuläre Neoplasie eine Operationsindikation dar.
BTS V – Verdacht auf Malignität (Dignitätsgruppe B2 nach ÖGZ und ÖGPath): Hierbei handelt es sich um Zellbilder mit Verdacht auf ein nichtfollikuläres Karzinom (z. B. papilläres Schilddrüsenkarzinom), wobei aufgrund des Zellbildes ein benigner Prozess nicht mit Sicherheit ausgeschlossen werden kann (z. B. Entzündung mit Atypien). In der Diagnose sollte eine genauere Zuordnung der suspizierten Entität erfolgen (z. B. v. a. papilläres Schilddrüsenkarzinom). Die Malignitätsrate liegt bei ca. 60–75 %, und eine operative Abklärung wird hier empfohlen.
BTS VI – maligne (Dignitätsgruppe C nach ÖGZ und ÖGPath): Bei Zytologien dieser Gruppe handelt es sich um ein malignes Zellbild, wobei in der Diagnose auch, wenn möglich, eine genaue Zuordnung erfolgen sollte (z. B. papilläres Schilddrüsenkarzinom). Die Malignitätswahrscheinlichkeit liegt hier zwischen 97 % und 99 % und stellt damit gewöhnlich eine Operationsindikation dar.
Resümee
Zusammenfassend hilft eine zeitgemäße und praxisrelevante Nomenklatur der Interpretation und Vergleichbarkeit pathologischer Befunde. Dies wird durch die evidenzbasierte Bethesda-Klassifikation im Bereich der Schilddrüsenzytologie möglich. Die Beibehaltung bewährter Klassifikationen (z. B. Dignitätsgruppenbewertung der ÖGZ/ÖGPath) ist dabei durchaus möglich und erleichtert auch die Kommunikation zwischen Klinikern und Pathologen.