Patienten mit chronischer Herzinsuffizienz – Schlafapnoe als relevanter unabhängiger Prognosefaktor
Nach Angaben der European Society of Cardiology leiden in etwa 10 Mio. Menschen in Europa an einer chronischen Herzinsuffizienz. Trotz derzeitiger medikamentöser Therapieoptionen beträgt die 1-Jahres-Mortalität dieser Erkrankung 24–28 %, die 5-Jahres-Mortalität liegt bei 45–60 %.
Die wesentlichsten Prädiktoren für die Prognose des einzelnen Patienten stellen der Schweregrad der Linksventrikelfunktionsstörung und das Ausmaß der neurohumoralen Aktivierung dar. Darüber hinaus hat neuen Studienerkenntnissen zufolge der Nachweis einer Schlafatemstörung prognostische Relevanz für das Langzeitüberleben der betroffenen Patienten.
OSAS oder CSA
Grundsätzlich muss man bei den Schlafatemstörungen zwischen den beiden Hauptgruppen, dem obstruktiven Schlafapnoesyndrom (OSAS) und der Cheyne-Stokes-Atmung (CSA), unterscheiden.
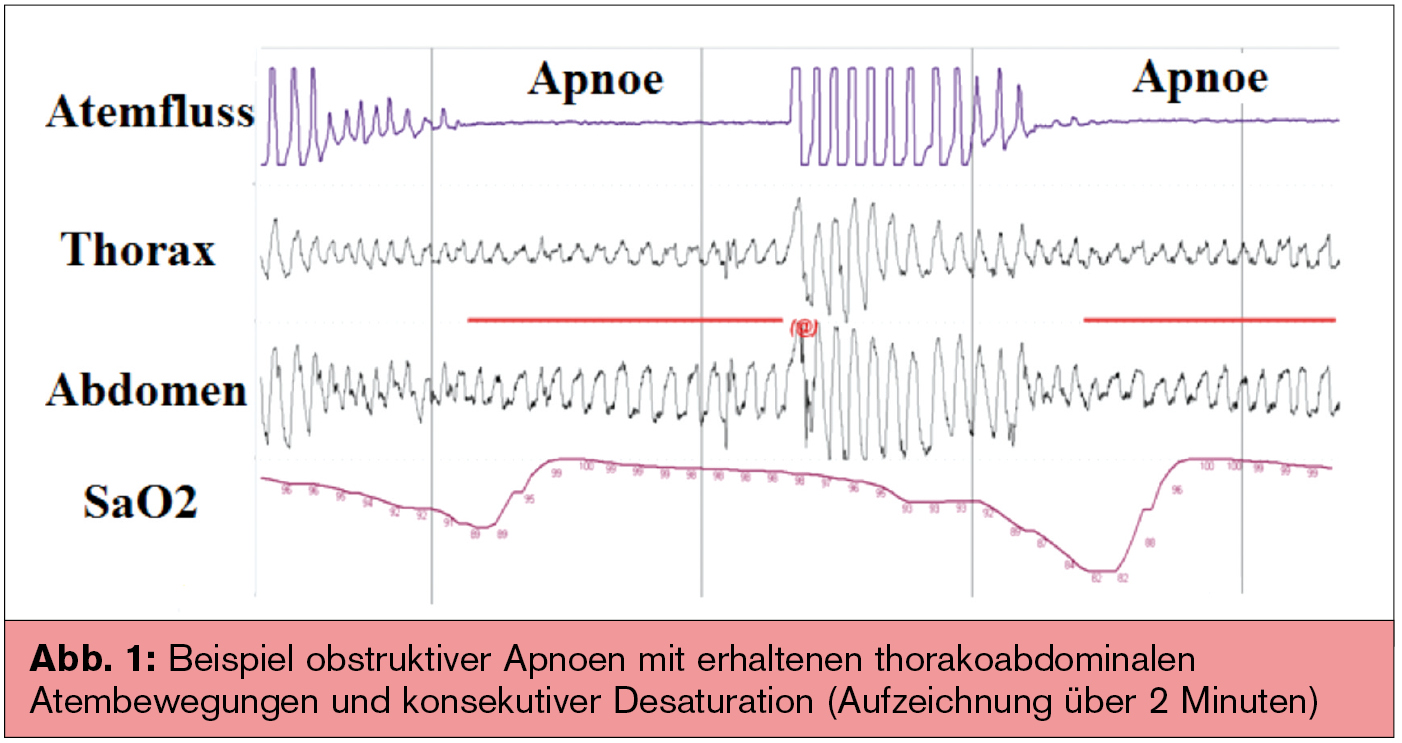
Das OSAS ist charakterisiert durch wiederholte Atemaussetzer im Schlaf, die durch eine mechanische Obstruktion auf Ebene der oberen Atemwege verursacht sind. Letztere können sich als simple Schnarchgeräusche bis hin zu lang anhaltenden Apnoephasen manifestieren und bis zu 50-mal pro Stunde Schlaf oder mehr auftreten. Der Hauptrisikofaktor für das OSAS ist die Adipositas, gefolgt von anderen Ursachen, die eine Einengung bzw. Kollapsibilität der oberen Atemwege begünstigen (Retrognathie etc.). Das Kardinalsymptom des OSAS ist die exzessive Tagesschläfrigkeit.
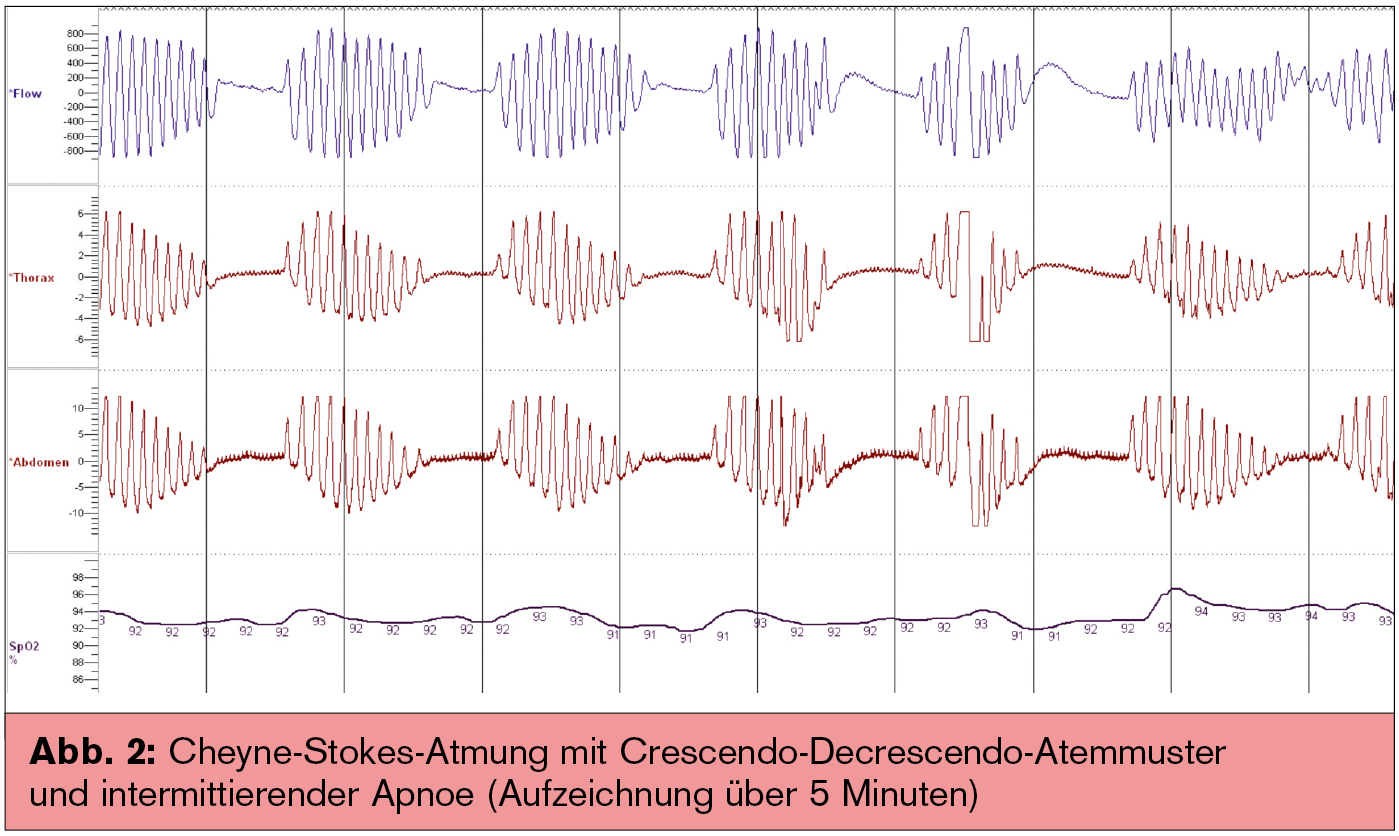
Bei der Cheyne-Stokes-Atmung hingegen handelt es sich um eine zentrale Schlafatemstörung, charakterisiert durch ein periodisches Atemmuster mit rhythmisch wechselnder, zu- und abnehmender Atemfrequenz und -Amplitude, unterbrochen von intermittierenden Apnoe-Perioden. Die Cheyne-Stokes-Atmung tritt nicht nur bei Patienten mit Herzinsuffizienz auf, sondern auch bei zentralnervösen Erkrankungen oder bei ansonsten „gesunden Personen“ mit Höhenaufenthalt. Die Symptome der CSA sind unspezifisch und entsprechen oft denen der Herzinsuffizienz.
Prävalenz
Eine der ersten größeren Prävalenzstudien wurde von Javaheri (Javaheri S. et al., Circulation 1998) durchgeführt. So konnten die Autoren bei 81 Patienten mit chronisch stabiler systolischer Herzinsuffizienz mittels nächtlicher Schlaflaboruntersuchung (Polysomnografie) bei 40 % der Patienten eine CSA nachweisen. Die bislang größte Studie wurde in Deutschland (Oldenburg O. et al., Eur J Heart Failure 2007) abgeschlossen. Dabei wurden 700 Patienten mit NYHA II–IV und einer LVEF < 40 % mittels Polygrafie untersucht. Bei 40 % der Patienten wurde eine CSA und bei 36 % ein OSAS attestiert. Somit zählen die Schlafatemstörungen zu den häufigsten Komorbiditäten der chronischen Herzinsuffizienz. Eine prospektive, multizentrische Studie zur Erhebung der Prävalenz der Schlafapnoe bei Patienten mit chronischer Herzinsuffizienz in Österreich (VISIFA-Studie) wurde kürzlich abgeschlossen und wird demnächst veröffentlicht.
Pathophysiologische Mechanismen
OSAS bei Herzinsuffizienz: Eine Reihe von Faktoren kann für die überzufällige Häufung von OSAS bei Patienten mit chronischer Herzinsuffizienz verantwortlich sein. Zum einen stellt die Adipositas einen gemeinsamen Risikofaktor für beide Erkrankungen dar. Zum anderen ist es denkbar, dass Patienten mit Herzinsuffizienz ein parapharyngeales interstitielles Ödem entwickeln, wodurch eine mechanische Einengung im Bereich der oberen Atemwege begünstigt wird. In pathophysiologischen Studien konnte ein nächtlicher Flüssigkeitsshift aus den Beinen in die oberen Atemwege beobachtet werden, wobei das Ausmaß dieses „rostral fluid shift“ mit dem Apnoe-Hypopnoe-Index (AHI, i. e. die Anzahl von Atemaussetzern pro Stunde Schlaf) korreliert (Redolfi S., Am J Respir Crit Care Med 2009).
Cheyne-Stokes-Atmung bei Herzinsuffizienz: Risikofaktoren für eine Cheyne-Stokes-Atmung bei Patienten mit chronischer Herzinsuffizienz sind männliches Geschlecht, fortgeschrittenes Alter, Vorhofflimmern und Hypokapnie. Der Mechanismus für die Entstehung der Cheyne-Stokes-Atmung ist multifaktoriell. Man nimmt an, dass Fluktuationen des arteriellen Kohlendioxidpartialdrucks über und unter die Apnoeschwelle an der Entstehung der CSA maßgeblich beteiligt sind. Dafür spricht, dass betroffene Patienten mit chronischer Herzinsuffizienz und Schlafatemstörung sowohl im Wachzustand als auch im Schlaf eine milde Hypokapnie aufweisen. Bei geringer Zunahme der Ventilation im Schlaf (z. B. durch Bewegung oder Weckphasen) wird der PaCO2 jedoch unter eine für diese Patienten kritische Apnoeschwelle gesenkt, wodurch eine zentrale Apnoe ausgelöst wird. Außerdem findet sich bei Patienten mit chronischer Herzinsuffizienz und CSA eine erhöhte zentrale und periphere Chemorezeptor-Empfindlichkeit für CO2. Gemeinsam mit der verlängerten Zirkulationszeit der Patienten kommt es durch diese Faktoren zu den für CSA typischen periodischen Atemmustern.
Klinische Relevanz
Die pathophysiologischen Konsequenzen von OSAS und CSA bei Patienten mit chronischer Herzinsuffizienz ähneln sich und inkludieren Hypoxämie, erhöhte Katecholaminfreisetzung, und systemische Inflammation. Darüber hinaus führt das OSAS zu wiederholten intrathorakalen Druckschwankungen, die zu einer „mechanischen Belastung“ des kardiovaskulären Systems mit erhöhter Nachlast führen. Eine Reihe von Untersuchungen konnte belegen, dass die oben angeführten Mechanismen mit einer erhöhten Prävalenz, aber auch Inzidenz von Herzrhythmusstörungen verbunden sind (Mehra R. et al., Arch Intern Med 2009). Vielmehr noch gibt es erste Daten dafür, dass Patienten mit Schlafapnoe und Herzinsuffizienz in Hinblick auf die Vorhofflimmern-Ablation häufig therapieresistent sind (Matiello M. et al., Europace 2010).
Unabhängiger Risikofaktor: Es überrascht daher nicht, dass der Nachweis einer Schlafatemstörung ein unabhängiger Risikofaktor für kardiovaskuläre Morbidität und Mortalität der betroffenen Patienten darstellt. Sin und Mitarbeiter (Sin D.D., Circulation 2000) konnten bei Patienten mit chronischer Herzinsuffizienz und nachgewiesener Schlafatemstörung einen signifikanten Unterschied im transplantfreien Überleben im Vergleich zu Patienten ohne nächtliche Atemaussetzer beobachten. Bemerkenswerterweise unterschieden sich die untersuchten Studiengruppen nicht in Hinblick auf Alter, Medikation oder das Ausmaß der Linksventrikelfunktionsstörung. Eine rezente Studie von Javaheri und Mitarbeiter (Javaheri S. et al., J Am Coll Cardiol 2007) bestätigte diese Ergebnisse anhand einer größeren Patientenfallzahl.
Auswirkungen der Herzinsuffizienz-Therapie
Wenn einmal die Diagnose einer Schlafatemstörung gestellt ist, ist es notwendig, die Behandlung der Herzinsuffizienz zu optimieren. Dies kann mittels Medikamenten (ACE-Hemmer, Betablocker, Diuretika etc.), Herzschrittmacher, kardialer Resynchronisationstherapie bis hin zur Herztransplantation erfolgen. Walsh et al. (Br Heart J 1995) konnten zeigen, dass die Behandlung der Herzinsuffizienz mit ACE-Hemmer bei Patienten mit milder bis moderater Herzinsuffizienz zu einer Verbesserung der Schlafqualität und zu einer Reduktion der nächtlichen Desaturationen führte. Bei bereits medikamentös ausreichend behandelten Patienten kann der Einsatz der kardialen Resynchronisationstherapie (Gabor et al., Eur Respir J 2005) eine weitere Verbesserung der Schlafatemstörung erzielen.
Auswirkungen der Behandlung der Schlafapnoe
Die nächtliche Masken-CPAP-(Continuous Positive Airway Pressure)-Therapie als Goldstandard in der Behandlung des OSAS ist nun schon seit vielen Jahren etabliert (Tab.). Durch die Anwendung einer nächtlichen nicht-invasiven positiven Überdruckbeatmung (nCPAP) kommt es zu einer deutlichen Verbesserung der Symptomatik, zu einer Verbesserung des Blutdruckprofils, zu einer Reduktion der Sympathikusaktivierung und folglich zu einer Abnahme der kardiovaskulären Morbidität und Mortalität (Marin J. et al., Lancet 2005). Aber auch bei Patienten mit CSA kann mittels CPAP eine klinisch relevante Verbesserung erzielt werden. Letztere ist in erster Linie auf eine Besserung der LVEF zurückzuführen. Die verbesserte kardiale Pumpfunktion ist durch die Vorlastsenkung als Folge einer Erhöhung der intrathorakalen Drücke zu erklären. Durch die CPAP-Applikation wird außerdem das interstitielle „Lungenödem“ verringert und dadurch eine Verringerung der Stimulation pulmonal-vagaler Afferenzen eingeleitet.
Im Gegensatz zur Behandlung des OSAS ist zur Behandlung der Cheyne-Stokes-Atmung jedoch keine individualisierte CPAP-Titration möglich, da sich der Behandlungseffekt auf Apnoen erst nach mehrwöchiger Therapie einstellt. Aus diesem Grund ist heute die autoadaptive Servoventilation* vorzuziehen. Hier ist eine auf den Patienten abgestimmte Optimierung der nächtlichen Ventilation möglich, wodurch die Elimination der nächtlichen Schlafatmungsstörung deutlich besser gelingt und sofort nachweisbar ist. Prospektive Studien mittels Servoventilation in großen Patientenkollektiven mit chronischer Herzinsuffizienz sind derzeit im Gange und werden in den nächsten beiden Jahren zur Verfügung stehen. Erste Kollektive aus nicht-randomisierten Studien zeigen einen deutlichen Überlebensvorteil für jene Patienten mit Herzinsuffizienz und Schlafapnoe, die einer Beatmungstherapie unterzogen werden (Jilek et al., Eur J Heart Fail 2011).
Die maschinelle Beatmungstherapie nächtlicher Schlafatemstörungen bei Patienten mit Herzinsuffizienz stützt sich auf eine rezente Behandlungsempfehlung der American Academy of Sleep Medicine (Aurora N, Sleep 2012; 35 [1]:17-40). Etwa 20 % der Patienten eignen sich nicht für eine nächtliche Maskentherapie. Als Ursache hierfür zählen die mit der Therapie auftretenden Nebenwirkungen, wie Druckstellen an der Haut, Mundtrockenheit, Rhinitis, und Klaustrophobie. Sowohl die CPAP-Therapie als auch die autoadaptive Servoventilationstherapie werden nach Vorlage eines entsprechenden Befundes von einem Schlaflabor von den Krankenkassen bezahlt, so dass für den Patienten in der Regel keine zusätzlichen Kosten entstehen.
Diagnose einer Schlafatemstörung
Auf Basis der existierenden Prävalenzzahlen und der prognostischen Bedeutung stellt sich die grundsätzliche Frage, ob nicht jeder Patient mit einer chronischen Herzinsuffizienz einer „Schlafatemuntersuchung“ zugeführt werden sollte. Patienten mit Herzinsuffizienz, die über Schnarchen, exzessive Tagesschläfrigkeit und/oder Fatigue bzw. schlechte Schlafqualität berichten, sollten daher diesbezüglich weiter untersucht werden. Neben den klassischen Symptomen sollte auch dann an eine nächtliche Schlafatemstörung gedacht werden, wenn nächtliche Angina pectoris und/oder Arrhythmien auftreten bzw. die Herzinsuffizienz therapieresistent scheint, i. e. der Patient mit Adipositas und Herzinsuffizienz wiederholt kardial dekompensiert.
Der Goldstandard zur Diagnose einer Schlafatemstörung ist die (stationäre) Polysomnografie inkl. EEG-, EMG- (Elektromyografie) und EOG-(Elektrookulogramm)-Aufzeichnung. Alternativ dazu bietet sich eine ambulante „Screeninguntersuchung“ mittels der Polygrafie (analog einer 24-Stunden-EKG-Untersuchung) an. Es handelt sich um eine vereinfachte Untersuchung inkl. Atemflussmessung, thorakoabdomineller Atembewegung, Sauerstoffsättigung, Lagesensor und EKG, jedoch ohne EEG (Abb. 1, Abb. 2). Neue Entwicklungen auf dem Gebiet implantierbarer Kardioverter-Defibrillatoren (ICDs) und Defibrillatoren zur kardialen Resynchronisation (CRT-Ds) ermöglichen zukünftig mittels intrathorakaler Impedanzuntersuchungen eine „In-vivo-Aufzeichnung“ nächtlicher Atemaussetzer bei Patienten mit chronischer Herzinsuffizienz (Incepta™, Boston Scientific) und könnten daher im klinischen Einsatz einen weiteren Baustein in der Diagnostik bzw. Verlaufsbeobachtung nächtlicher Schlafatemstörungen liefern.
ZUSAMMENFASSEND kann gesagt werden, dass in der ganzheitlichen (interdisziplinären) Evaluierung von Patienten mit chronischer Herzinsuffizienz die Wahrscheinlichkeit einer nächtlichen Atmungsstörung berücksichtigt werden sollte. Patienten mit Herzinsuffizienz und Schlafapnoe sind einem erhöhten Risiko für Mortalität ausgesetzt, eine entsprechende Therapie kann Morbidität und Linksventrikelfunktion verbessern.
* Bei der autoadaptiven Servoventilation handelt es sich um eine neue Beatmungsform, die neben der CPAP-Therapie im Exspirium, eine inspiratorische Druckunterstützung in Phasen der Hypoventilation anbietet. Die Beatmungsdruckunterstützung variiert dabei in Abhängigkeit vom erzielten Tidalvolumen und ermöglicht so eine Harmonisierung der paCO2-Werte und somit ein Verschwinden der Cheyne-Stokes-Atmung.