Ovarialfunktion und Ovarialreserve
Der in der Fetalzeit angelegte “Pool” von Eizellen beginnt sich bereits pränatal zu entleeren. Nach der Geburt nimmt die Zahl der Primordialfollikel kontinuierlich ab. In der reproduktiven Phase werden pro Zyklus 40 bis über 100 Follikel “verbraucht”. Der Follikelpool als Ausdruck ovarieller Reserve nimmt somit mit dem Alter ab.
Basishormonstatus und Ovarialfunktion
Neben der klinischen ist auch eine endokrinologische Überprüfung der Ovarialfunktion möglich. Mit dem so genannten Basishormonstatus zwischen dem 3. und 5. Zyklustag, der die Gonadotropine FSH (follikelstimulierendes Hormon) und LH (luteinisierendes Hormon) sowie den Östrogenspiegel umfasst, ist eine grobe Abschätzung der Ansprechbarkeit der Ovarien auf Gonadotropine möglich.
Um weitere Einflussfaktoren auf die Ovarialfunktion abzuklären, ist auch das Prolaktin und das TSH (Thyreoidea-stimulierendes Hormon) mit zu bestimmen. Ein Spiegel funktionierender Ovarien ist auch ein Progesteronwert von mehr als 3 ng/ml (z. B. am 21. Zyklustag bei einem Zyklus von 28 Tagen). Er macht eine stattgehabte Ovulation evident.
Die Beurteilung der Ovarialfunktion ist ein Schlüssel zur Feststellung weiblicher Fruchtbarkeit. Die klassische vorzeitige Erschöpfung der Eierstöcke im Sinne einer Ovarialinsuffizienz ist mit einer Inzidenz von einem Prozent relativ gering, sie steigt aber durch die Erfolge der Onkologie “iatrogen” an.
Der FSH-Spiegel ist eine etwas grobe Methode zur Bestimmung der Ovarialfunktion und Ovarialreserve.
Für Frauen, die älter als 35 Jahre sind, und für jüngere Frauen mit vorzeitiger Menopause ist die ovarielle Reserve am Tag 3 über einen FSH-Spiegel nur orientierungsgemäß zu bestimmen. Zu viele Einflussfaktoren verursachen Schwankungen.
CCCT: Häufig wird auch der Clomiphene Citrate Challenge Test (CCCT) verwendet. 100 mg Clomiphenzitrat werden von Tag 5 bis Tag 9 verabreicht und FSH-Spiegel am Tag 3 und am Tag 10 sowie ein Östradiolspiegel am Tag 3 gemessen. Basis der Bewertung ist das Faktum, dass Frauen mit einer ausreichenden Eierstockreserve eine entsprechende Produktion von Östrogenen durch die kleinen Follikel des frühen Zyklus aufweisen, um das FSH auf einem niedrigen Level zu halten.
Frauen mit einem reduzierten Pool an Follikeln und Oocyten haben eine insuffiziente Produktion von Östrogen und damit ein reduziertes Vermögen die Ausscheidung von FSH in der Hypophyse zu hemmen. Deshalb steigt FSH schon früh im Zyklus an.
Diese Tests sind nicht aussagekräftig genug, um Fertilität sicher vorauszusagen. Sie dienen aber dazu, höchst abnorme Resultate wie ein FSH von über 20 mIU/ml zu selektionieren, die eine Schwangerschaft mit eigenen Eizellen äußerst unwahrscheinlich machen. Eine Tag-3-FSH-Konzentration unter 10 mIU/ml weist auf eine adäquate ovarielle Reserve hin, mit 10-15 mlU/ml befindet man sich in einem Borderline-Bereich.
Erhöhte basale Östradiolwerte am Tag 3 (> 50 pg/ml) entstehen durch eine zu frühe Follikelrekutierung. Sie verhindern ihrerseits die FSH-Ausschüttung und maskieren die Zeichen einer verminderten ovariellen Reserve bei perimenopausalen Frauen. Das ist der Grund, weswegen FSH- und Östradiolspiegel nur gemeinsam bewertet werden sollen. Eine alleinige FSH-Testung kann auch eine falsch -negative sein.
Östradiol am Tag 10 im CCCT zu messen ist nicht aussagekräftig, weil der Östradiolspiegel nur die Bandbreite der ovariellen follikulären Antwort auf Clomiphen innerhalb von 5 Tagen wiedergibt, aber nicht die ovarielle Reserve abbildet.
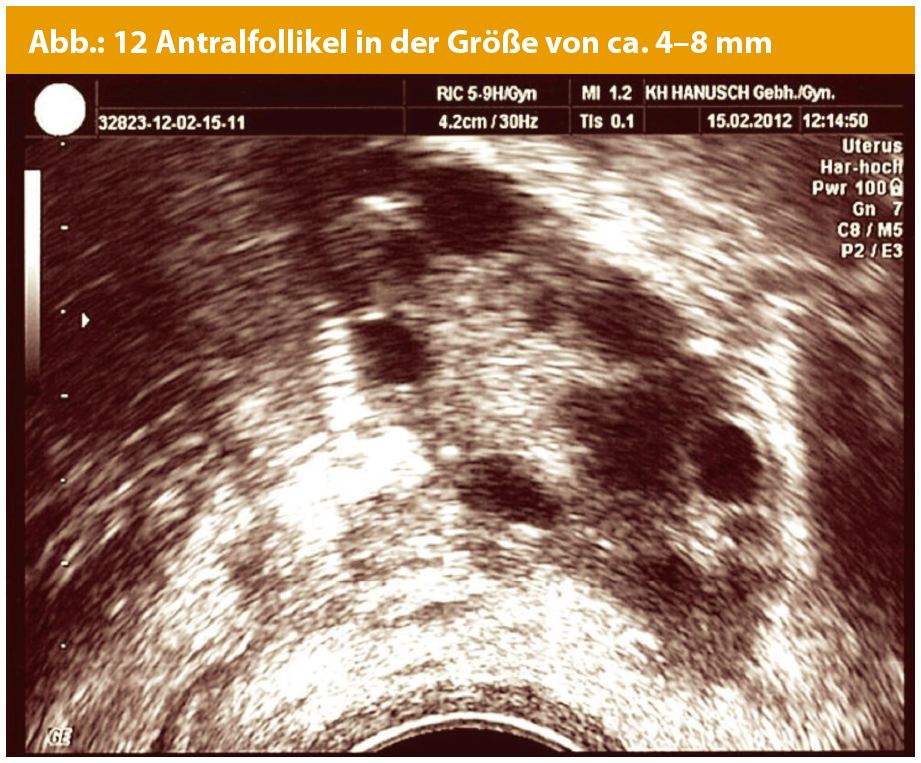
Sonographische Antralfollikelzählung
Die sonographische Antralfollikelzählung (Antral Follicle Count = AFC) misst die Anzahl der antralen Follikel (zwischen 2 und 10 Millimetern im Durchmesser) und ist ein guter Prädiktor der ovariellen Reserve sowie der ovariellen Antwort auf hormonelle Stimulation. Sie kann aber nicht die Oocytenqualität und etwaige Chancen, über IVF (In-vitro-Fertilisation) schwanger zu werden, abschätzen.
Die Validität der Methode ist gut, aber sehr vom Operator (Sonographer) abhängig.
Das Antimüllerian Hormone
Das Antimüllerian Hormone (AMH) ist ein Glykoprotein der TGF-β-Familie. Es ist ein Sekretionsprodukt der Granulosazellen der primären, sekundären und frühen antralen Follikeln. Besonders jene zwischen 2 und 5 mm Größe reflektieren das zirkulierende AMH. AMH hemmt die Rekutierung von Follikeln und die Follikelselektion und führt zu einer geringeren Empfindlichkeit gegenüber FSH. AMH reguliert den Follikelverbrauch im Leben einer Frau. Wenn durch Anomalien von Rezeptoren das AMH nicht richtig wirken kann, kommt es zu einem beschleunigten Follikelverlust, was Ursache einer primären Ovarialinsuffizienz sein kann.
AMH korreliert negativ mit dem Verlust von Follikeln und dem Alter der Frau. In anderen Worten, je höher das AMH, desto höher die Follikelzahl. AMH ist der valideste Parameter für die Beurteilung der Zahl antraler Follikel. Es zeigt kaum Zyklusschwankungen und wird durch orale Kontrazeptiva oder eine Schwangerschaft nicht beeinträchtigt.
Bei ovarieller horomoneller Stimulation kommt es initial (innerhalb von 1 bis 2 Tagen) zu keinen AMH-Veränderungen, danach allerdings zu einem Abfall von AMH. In verschiedenen Studien zeigten sich im Rahmen von IVF gute Korrelationen zur gewonnenen Eizellzahl und zum Eintreten einer Schwangerschaft sowie auch einer Lebendgeburt.
AMH fällt unter einer Chemotherapie durch die Zerstörung von aktiven Follikeln relativ schnell ab. Für Patientinnen mit Chemo- sowie Strahlentherapie ist die AMH-Beurteilung vor und nach diesen bezüglich Fertilitätschancen der wichtigste Parameter. Mit einer Kinderwunschbehandlung ist frühestens ab dem Wiedereinstieg des AMH 4-6 Monate nach einer Chemotherapie zu beginnen.
Zur Beurteilung von Störungen der Geschlechtsdifferenzierung (ein hoher AMH-Spiegel weist im Neugeborenenalter auf das Vorliegen von Hodengewebe hin) ist AMH ebenfalls ein wichtiger Indikator. Außerdem ist AMH ein wesentlicher Marker zur Verlaufsbeobachtung von Ganulosazelltumoren. Die Referenzbereiche von AMH sind nicht in einer fixierten Bandbreite einzuordnen.
Bei endokrinologisch unauffälligen Patientinnen ist ein AMH im Median von 2,1 ng/ml beschrieben, bis zum Alter von 35 Jahren ist es eher höher als 2 ng/ml, später niedriger. PCO-Syndrom- Patientinnen haben deutlich höhere Spiegel, was auch als diagnostischer Parameter genützt werden kann (mehr als 5 ng/ml bis über 15 ng/ml). Ein AMH < 1 ng/ml deutet auf eine deutlich niedrigere Follikel- bzw. Eizellzahl im Rahmen einer Kinderwunschbehandlung hin.
Wann ist eine AMH-Bestimmung indiziert? Bei Kinderwunschpatientinnen, bei denen sich frühfollikulär oder bei einem Alter unter 35 Jahren ein FSH im oberen Referenzbereich (über 8 mIU/ml) zeigt, kann AMH dazu dienen, die ovarielle Reserve genau einzuschätzen.
Fazit: Ovarialfunktion und ovarielle Reserve sind über die Klinik des Menstruationszyklus, über einen Basishormonstatus zwischen 3. und 5. Zyklustag sowie den Clomiphene Citrate Challenge Test in groben Zügen bestimmbar. Ein niedriges AMH von < 1 ng/ml oder auch eine niedrige Antralfollikelzahl im AFC (weniger als 10 Follikel bei Frauen bis 34 Jahren, weniger als 8 bei Frauen zwischen 35 und 40 Jahren) sind ein eindeutiger Hinweis auf eine verminderte ovarielle Reserve.
Literatur bei den Verfassern