Management von Nausea und Emesis bei Krebspatienten
Nausea: Drang zum Erbrechen; Emesis: Fremdreflex
Um die komplexen therapeutischen Optionen besser verstehen zum können, sollen zunächst die Begriffe Nausea und Emesis näher erläutert werden.
Nausea ist eine mit dem Drang zu Erbrechen verbundene Empfindung, die von kortikalen Bereichen ausgeht und von vegetativer Symptomatik begleitet wird.
Emesis stellt einen komplexen Fremdreflex dar, der durch periphere (viszerale oder vestibuläre) und zentrale Afferenzen oder direkte Aktivierung der Chemorezeptortriggerzone ausgelöst wird. Dies resultiert in explosionsartigem Auswurf von Mageninhalt durch Kontraktionen von Abdominal- und Thoraxwandmuskulatur. In diesem Zusammenhang sollen auch die Begriffe Regurgation und Rumination erwähnt werden. Bei der Regurgation kommt es zur Rückpassage von Mageninhalt in den Mund, Rumination bedeutet wiederholte Regurgation von Mageninhalt mit Wiederkäuen desselben, wie es z. B. bei Kühen oder bestimmten Essstörungen vorkommt.
Brechzentrum: „Schrittmacher“ und Koordinator
Die Mechanismen, die zur Empfindung der Übelkeit führen, sind noch weitgehend unverstanden. Vermutlich ist die Großhirnrinde daran beteiligt. Elektroenzephalographische Studien zeigten eine Aktivierung von temporokortikalen Regionen mit Induktion von Übelkeit.
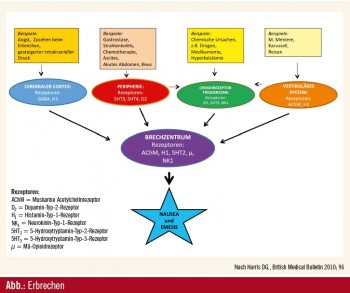
Das Erbrechen wird durch zwei Bereiche im Hirnstamm kontrolliert: dem Brechzentrum in der Formatio reticularis in der Medulla oblongata sowie der Chemorezeptortriggerzone in der Area postrema.
Das Brechzentrum in der Medulla oblongata ist ein diffuses neuronales Netzwerk innerhalb der Blut-Hirn-Schranke, das als „Schrittmacher“ und Koordinator für das Erbrechen dient. Es enthält Rezeptoren für 5-HT2, Acetylcholin (ACh), Opioide (µ), Histamin (H1) und NK1. Gereizt wird es durch Inputs aus der Chemorezeptortriggerzone, dem Vestibularsystem, dem X. Hirnnerv (N. vagus), dem vagalen enteralen System sowie von Signalen aus der Großhirnrinde und dem ZNS.
Die Chemorezeptortriggerzone (CTZ, Area postrema) liegt am Boden des 4. Ventrikels im Gehirn und ist ein zirkumventrikuläres Organ, das außerhalb der Blut-Hirn-Schranke liegt. Stimuliert wird es von Chemikalien in der Spinalflüssigkeit und im Blut, aber auch von vestibulären und vagalen Afferenzen. Die CTZ enthält Rezeptoren für Dopamin (D2), Serotonin (5-HT3), Acetylcholin (ACh) und NK1.
Verschiedene Neurotransmitter sind daher an Nausea und Emesis mitbeteiligt (Abb.). Die Blockade dieser Neurotransmitter kann daher das Auftreten von Nausea und Emesis verhindern oder abschwächen.
Die Reizung des Brechzentrums führt schließlich über Aktivierung des motorischen, parasympathischen und sympathischen Nervensystems zum Akt des Erbrechens (Abb.).
Akt des Erbrechens
Der Akt des Erbrechens wird durch Stimulation des Brechzentrums herbeigeführt. Hierbei werden zunächst verschiedene Hirnstammkerne aktiviert, welche die Emesis initiieren. Der Nucleus tractus solitarii, der dorsale Vaguskern und die Phrenicus-Kerne kontrollieren Rachen-, Gesichts- und Zungenbewegungen und führen zur Einleitung des Erbrechens.
Die somatische und die viszerale Muskulatur bewirken eine Entspannung des Magenfundus und des gastroösophagealen Sphinkters und erhöhen somit den Druck durch Brust- und Bauchwandmuskeln. Die Cardia schiebt sich über das Zwerchfell, der Kehlkopf wird nach oben gedrückt, um die Luftröhre zu schützen, der weiche Gaumen wird angehoben, um den Nasopharynx zu schützen. Dies alles resultiert in explosionsartigem Auswurf von Mageninhalt durch den Mund. Gleichzeitig führt die Erregung des Brechzentrums zu einigen Maßnahmen, die den Körper vor dem Erbrochenen schützen sollen: gesteigerter Speichelfluss schützt den Zahnschmelz vor der Magensäure, und unwillkürliches Einatmen vor dem Erbrechen schützt vor Aspiration.
Evolutionär gesehen stellt der Akt des Erbrechens einen Schutz des Körpers gegen Vergiftungen dar.
Anhand der oben angeführten Erklärung über die Entstehung des Erbrechens erscheint nun verständlich, warum verschiedene Reize als Aktivatoren für Emesis dienen können. Gedanken, Gerüche und Anblicke können das Brechzentrum über die Hirnrinde aktivieren (dies spielt eine Rolle beim antizipatorischen Erbrechen; siehe unten). Eine Reizung des N. vagus, z. B. durch eine Feder im Rachenraum, kann ebenso Erbrechen auslösen. Erkrankungen des Innenohrs oder Labyrinths führen über Histaminrezeptoren zum Erbrechen. Reizstoffe im Magen wie Gifte oder Chemotherapeutika lösen ebenfalls Erbrechen aus. Die Wahrnehmung von schädlichen Substanzen, seien es körperfremde Gifte (wie z. B. Chemotherapeutika) oder körpereigene Substanzen (wie z. B. zu viel Kalzium oder Harnstoff) über die Area postrema ebenfalls.
Klinik des Erbrechens
Anhand des Einsetzens und der Dauer des Erbrechens kann man Rückschlüsse auf die Ursachen ziehen. Akutes Erbrechen wird oft durch Medikamente, Gifte oder gastrointestinale Infektionen hervorgerufen. Chronisches Erbrechen weist oftmals auf Stoffwechselerkrankungen hin.
Zusätzliche Symptome geben Hinweise auf Begleiterkrankungen oder dem Erbrechen zugrunde liegende Pathologien. Bauchschmerzen, die nach Erbrechen kurzfristig besser werden, sprechen zum Beispiel für einen Ileus oder ein Ulkus. Bei Pankreatitis oder Cholezystitis kommt es nach dem Erbrechen oft nicht zur Besserung. Fieber weist oft auf einen gastrointestinalen Infekt hin. Kopfschmerzen oder Gesichtsfeldausfälle weisen auf ein zerebrales Geschehen hin, zusätzliche Vertigo oder Tinnitus auf labyrinthäre Erkrankungen.
Auch der Morphologie des Erbrochenen sollte Beachtung geschenkt werden. So weisen unverdaute Speisereste auf ein Zenker-Divertikel oder eine Achalasie hin, verdaute Speisen hingegen auf eine Gastroparese. Galliges Erbrochenes weist oft auf Magenobstruktion hin. Hämatemesis auf ein Ulcus, malignes Geschehen oder ein Mallory-Weiss-Syndrom. Fäkulentes Erbrechen (Miserere) ist auf eine oft mechanische Darmobstruktion hinweisend. Berichtet der Patient von anfallartigem, schwallartigem Erbrechen, so deutet dies oft auf erhöhten Hirndruck hin.
Differenzialdiagnose
Gerade bei Patienten mit einer fortgeschrittenen Krebserkrankung ist es besonders wichtig, Überlegungen anzustellen, welche Ursachen für Übelkeit und Erbrechen in Frage kommen könnten. Nicht nur Chemotherapie, Strahlentherapie oder fortschreiten der Grunderkrankung kommen dafür in Frage. Eine genaue differenzialdiagnostische Analyse ergibt oft wichtige Hinweise für auslösende Faktoren oder zusätzliche Auslöser von Nausea und Emesis.
Diagnostische Maßnahmen
Zur genaueren Differenzierung des Erbrechens sowie zur Erhebung der Ursache sind einige diagnostische Untersuchungen unerlässlich. Eine gründliche Anamnese und genaue körperliche Untersuchung lassen oft schon Rückschlüsse über die Genese des Erbrechens zu. Das Labor sollte neben den Routineparametern (Blutbild, klinische Chemie, CRP) auch den Eisenstatus und die Pankreasenzyme erfassen. Diverse endokrinologische Parameter können bei Verdachtsdiagnosen erhoben werden. Bei Vorliegen von Diarrhö ist an eine Stuhlkultur zu denken.
Bei den bildgebenden Verfahren sollte bei klinischem Verdacht auf Ileus oder Perforation ein Abdomen-leer-Röntgen durchgeführt werden. Zur weiteren Abklärung abdomineller, insbesondere hepatischer Pathologien ist an eine Sonografie des Abdomens zu denken. Bei weiteren Fragestellungen kann eine Computertomografie bzw. bei besonderen Indikationen eine Magnetresonanztomografie des Abdomens durchgeführt werden. Besonders bei Patienten mit schwallartigem Erbrechen, die an einer malignen Erkrankung leiden, die auch zerebral metastasieren kann, sollte eine Computertomografie des Gehirns, besser noch eine Magnetresonanztomografie durchgeführt werden. Bei anhaltender Übelkeit oder Verdacht auf Ulzera sollte auch an eine endoskopische Untersuchung gedacht werden.
Komplikationen
Die häufigste Komplikation von Nausea und Emesis ist die Dehydratation, der generell mit intravenöser Flüssigkeitssubstitution entgegengewirkt werden kann. In seltenen Fällen kann heftige Emesis bis zur Ruptur der Speiseröhre (Boerhaave-Syndrom) oder Schleimhautrissen (Mallory-Weiss-Syndrom) führen. Regelmäßiges Erbrechen führt in Folge zu Mangelernährung, Karies und sogar zur metabolischen Alkalose. Nicht selten leiden Patienten mit rezidivierendem Erbrechen an Aspirationspneumonien.
Besonders erwähnenswert bei Krebspatienten ist, dass die Non-Compliance unter Chemotherapie zu schlechteren Ansprechraten und somit schlechterem Gesamtüberleben führen kann.
Nicht zuletzt deswegen muss eine adäquate Erhebung der Ursachen von Nausea und Emesis in Folge mit adäquater antiemetischer Therapie durchgeführt werden.
Therapie des Erbrechens
Symptomorientierte Therapie: Eine wichtige Säule in der Behandlung von Emesis stellt die intravenöse Rehydrierung dar.
In weiterer Folge sollte versucht werden, die Ursache für die Nausea und Emesis zu beseitigen, Korrigierbares also zu korrigieren.
Falls dies nicht gelingt, müssen spezifische Medikamente zur Unterdrückung des auslösenden Reizes eingesetzt werden (siehe Kapitel: Ausgewählte Antiemetika).
Therapie durch Antiemetika: Antiemetika sind Substanzen, die die Wirkung von emetogenen Substanzen an den entsprechenden Rezeptoren vermindern oder sogar blockieren. Sie werden häufig in der Behandlung von therapieassoziierter Nausea und Emesis eingesetzt.
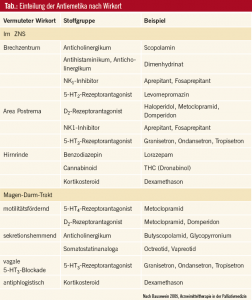
Wie bereits oben erwähnt, wird das Erbrechen über Neurorezeptoren und Chemorezeptoren in der Peripherie, im Brechzentrum und in der Area postrema gesteuert. Hier finden sich Rezeptoren für Serotonin, Histamin, Dopamin, Acetylcholin, Opioide, Substanz P und eine ganze Anzahl an weiteren endogenen Neurotransmittern. Antiemetika blockieren kompetitiv die Rezeptoren für diese Substanzen und hemmen somit die Stimulation von Nausea und Emesis. Manche Antiemetika blockieren sogar verschiedene Rezeptorklassen und sind in ihrem Einsatzgebiet daher breiter.Die Antiemetika können entsprechend ihrem Wirkort (Tab.) oder ihrer Substanzklasse eingeteilt werden.
Die Affinität der Antiemetika zu den jeweiligen Rezeptoren ist unterschiedlich. Einige Antiemetika binden sogar an mehrere Rezeptoren, sodass sie ein breiteres Wirkungsspektrum aufweisen.
Ausgewählte Antiemetika
Levomepromazin (Nozinan®)
Levomepromazin gehört zur Gruppe der Phenothiazine. Es wirkt antagonistisch an D2, H1, Muskarin- und 5-HT2-Rezeptoren und ist somit das am breitesten wirkende Antiemetikum. Indiziert ist es bei starker Übelkeit als Antiemetikum der zweiten Wahl, vor allem deshalb, weil es sehr stark sedierend und anticholinerg wirkt. Es wird bei anhaltender Übelkeit in einer Dosierung von
- 5 bis 10 mg p. o. bzw. s. c. verabreicht.
Besondere Vorsicht ist bei Parkinsonismus, Hypotonie und Epilepsie geboten.
Haloperidol (Haldol®)
Haloperidol ist ein Butyrophenon. Es wirkt antagonistisch am D2-Rezeptor. Haloperidol als Antiemetikum findet seinen Einsatz bei arzneimittelinduziertem Erbrechen, vor allem durch Opioide; aber auch bei Emesis durch Elektrolytstörungen ist es hilfreich. Ansonsten ist es bekannt im Einsatz gegen schwere Psychosen, hier allerdings in viel höheren Dosierungen als im antiemetischen Gebrauch.
An Nebenwirkungen sind extrapyramidale Symptome, tardive Dyskinesien, Hypotonie, Leberfunktionsstörungen, Blutbildveränderungen und das maligne neuroleptische Syndrom zu beachten. Bei Übelkeit werden 1,5–3 mg per os bzw. s. c. verabreicht. Das Medikament sollte nicht beim M. Parkinson eingesetzt werden.
Metoclopramid (Paspertin®)
Metoclopramid zählt zur Gruppe der Benzamide. Es wirkt antagonistisch an D2-, 5 HT3– und 5-HT4-Rezeptoren. Metoclopramid ist induziert bei Emesis bedingt durch Gastrostase, Chemotherapie oder Bestrahlung. Besondere Vorsicht ist bei der gleichzeitigen Gabe von Anticholinergika, anderen HT3-Antagonisten, Antidepressiva und Neuroleptika geboten. Aber auch bei jüngeren Patienten (< 30 J) soll es nicht unbedacht verwendet werden, da hier das Auftreten von extrapyramidalen Nebenwirkungen häufiger vorkommt. Als Gegenmittel kann hier jedoch Biperiden (Akineton®) i. v. eingesetzt werden. Metoclopramid kann auch zur Benommenheit und Ruhelosigkeit führen. Als gravierendste Nebenwirkung ist auch hier das maligne neuroleptische Syndrom zu werten.
Verwendet wird es in einer Dosierung von
- 10 mg per os bis zu 4-mal tgl.,
- 100 mg s. c. über 24 Stunden oder
- 25–50 mg i. v.
5-HT3-Antagonisten
Ondansetron (Zofran®), Granisetron (Kytril®), Dolasetron (Anzemet®), Palonosetron (Aloxi®) und Tropisetron (Navoban®): Die so genannten 5-HT3-Rezeptorantagonisten oder auch Serotoninantagonisten wurden in den frühen 1990er-Jahren als Antiemetika entdeckt und werden hauptsächlich gegen chemotherapieinduzierte Übelkeit verwendet. Aber auch bei postoperativer Übelkeit und bei Übelkeit durch Migräne finden sie ihre Anwendung. Zytostatika führen zur massiven Freisetzung von Serotonin aus den enterochromaffinen Zellen im Gastrointestinaltrakt. Die Wirkung der 5-HT3-Antagonisten erklärt sich durch die Verdrängung von Serotonin, das aus den enterochromaffinen Zellen des Gastrointestinaltrakts freigesetzt wird, von seinen Rezeptoren im ZNS und im Gastrointestinaltrakt (siehe oben). Dadurch wird der emetogene Reiz in der Area postrema und in höheren Gehirnzentren unterbunden.
Die verschiedenen 5-HT3-Antagonisten dürften sich in ihrer Wirksamkeit kaum wesentlich unterscheiden, bis auf Palonosetron, das eine längere Wirkdauer aufweist. Auch Metoclopramid und Kokain sind schwache 5-HT3-Antagonisten, jedoch wesentlich weniger potent als die neuen Substanzklassen.
Ein weiteres Einsatzgebiet für die oben genannten 5-HT3-Antagonisten dürfte chronischer Juckreiz bei renaler Insuffizienz sein.
Die häufigsten Nebenwirkungen der 5-HT3-Antagonisten sind Obstipation, Cephalea und selten Diarrhö, gelegentlich erhöhte Leberfunktionsparameter.
Die 5-HT3-Antagonisten der 1. Generation, Ondansetron, Granisetron, Tropisetron und Dolasetron unterscheiden sich hauptsächlich durch ihre Dosierung bzw. unterschiedliche Pharmakokinetik voneinander.
Die Dosierungen sind wie folgt:
- Ondansetron 8 mg 2-mal tgl. per os, i. v.
- Granisetron 2 mg 1-mal tgl. per os, 1 mg i. v.
- Tropisetron 5 mg 1-mal tgl. pe os, 2 mg i. v.
- Dolasetron 200 mg 1-mal per os bzw. 100 mg i. v.
- Palonosetron 0,25 mg i. v. vor Chemotherapie
Palonosetron ist ein 5-HT3-Antagonist der 2. Generation, der eine höhere Affinität zu den 5-HT3-Rezeptoren aufweist als die Antagonisten der 1. Generation. Es wurde von der FDA 2003 zugelassen. Durch eine Konfirmationsänderung des Rezeptors wird es in die Zellen internalisiert.
Seine Halbwertszeit beträgt im Durchschnitt 40 Stunden, zirka vier bis fünf Mal länger als die „alten“ Antagonisten. Er wirkt daher auch besser auf die „verzögerte“ Übelkeit (siehe unten).
NK1-Rezeptorantagonisten
Die im Jahre 1931 in Pferdegehirnen entdeckte Substanz P wurde in den 1980er-Jahren als Neurokinin identifiziert. Substanz P bewirkt eine starke Erweiterung der Blutgefäße und steigert die Durchlässigkeit der Gefäßwand. Zudem bewirkt sie eine Steigerung der Sensitivität der Schmerzneurone im Rückenmark. Das Brechzentrum in der Medulla oblongata enthält hohe Konzentrationen von Rezeptoren für die Substanz P, die so genannten Neurokinin-1-Rezeptoren (NK1). Die Blockade von Substanz P an den Rezeptoren kann daher Nausea und Emesis unterbinden. In den 1980er-Jahren wurde der erste NK1-Rezeptorantagonist etabliert. 2003 erfolgte von der FDA die Zulassung eines oralen NK1-Inhibitors als Antiemetikum, Aprepitant (Emend®). Darauf folgte 2008 die FDA-Zulassung von Fosaprepitant (Ivemend®), einem intravenösen NK1-Inhibitor. NK1-Inhibitoren wirken vor allem auf die verzögerte Übelkeit, die erst Stunden nach der Applikation der Chemotherapie auftritt. Bei hochemetogenen Chemotherapieformen sollten NK-Inhibitoren zusätzlich eingesetzt werden.
Zu beachten ist, dass Aprepitant vom Cytochrom P450 metabolisiert wird, dies ist bei der gleichzeitigen Verwendung von z. B. Dexamethason zu beachten.
An Nebenwirkungen treten Kopfschmerzen und bei Aprepitant Schmerzen an der Einstichstelle auf.
- Aprepitant wird am Tag 1 mit 125 mg per os und an den Tagen 2 und 3 mit 80 mg dosiert.
- Fosaprepitant wird am Tag 1 mit 150 mg i. v. dosiert.
Für Aprepitant konnte gezeigt werden, dass es bei hochemetogener Chemotherapie in Kombination mit einem 5-HT3-Antagonisten und Kortikosteroiden zu 80–90 % Ansprechraten kommt, vor allem in Bezug auf die verzögerte Übelkeit und bei anthrazyklinhältiger Chemotherapie zu Ansprechraten bis zu 80 %. Für Fosaprepitant konnte gezeigt werden, dass die einmalige intravenöse Gabe der dreimaligen Per-os-Applikation von Aprepitant um nichts nachstand.
Kortikosteroide
Der antiemetische Wirkungsmechanismus der Kortikosteroide bleibt unklar. Gesichert ist ihre antiemetische Wirkung in Kombination mit anderen Antiemetika bei milder bis moderat emetogener Chemotherapie. Vermutlich reduzieren Kortikosteroide die Permeabilität der Area postrema und der Blut-Hirn-Schranke und führen dadurch zur Verminderung von Emesis. Bei Gehirnmetastasen dürfte ein Abschwellen des umgebenden Ödems einen positiven Effekt auf durch erhöhten Hirndruck bedingtes Erbrechen haben.
Möglicherweise dezimieren Kortikosteroide auch die inhibitorische Wirkung von Gamma-Aminobuttersäure. Bewiesen ist jedoch die Potenzierung der antiemetischen Wirkung in Kombination mit 5-HT3-Rezeptorantagonisten und NK1-Inhibitoren . Indiziert ist die Gabe von 8 bis 40 mg Dexamethason i. v./per os bei hochemetogener und moderat emetogener Chemotherapie in Kombination mit anderen Antiemetika. An Nebenwirkungen sind Immunsuppression, Muskelschwäche, Hyperglykämie, Magenreizungen, Schlafstörungen und Aggravierung von Psychosen anzuführen. Bei der raschen Applikation von Dexamethason wurde Schleimhautbrennen als störende Nebenwirkung angegeben.
Cannabinoide
Cannabinoide entfalten ihre Wirkung als Rezeptorantagonisten auf dem CB1-Rezeptor im ZNS. Die Datenlage bezüglich des Einsatzes von Cannabinoiden als Antiemetika ist spärlich und bezieht sich auf wenige Fallberichte.
Sie können als Zweitlinientherapie bei therapierefraktärer Nausea und Emesis versucht werden. Bei älteren Menschen und Patienten mit psychotischen Episoden in der Anamnese ist jedoch Vorsicht geboten. Dronabinol sollte vorsichtig mit besonderem Augenmerk auf Nebenwirkungen eintitriert werden. Besonders zu achten ist auf Benommenheit, Schwindel, Euphorie, Mundtrockenheit, Ataxie, Sehstörungen, Konzentrationsstörungen, Verwirrtheit, Halluzinationen, Psychosen, Depression, Tremor, Tachykardie oder Bauchschmerzen.
Die Dosierung ist wie folgt
- Initial 2,5–5 mg per os, aufgeteilt auf 2–3 Einzelgaben, bis zu 20 mg ölige Dronabinol-Tropfen 2,5 %; 10 g = 250 mg.
Benzodiazepine
Benzodiazepine entfalten ihre Wirkung durch Bindung an GABA-Rezeptoren und verstärken so die inhibitorische Wirkung von Gamma-Aminobuttersäure. Dadurch wirken sie anxiolytisch, antiaggressiv, schlafinduzierend, sedierend und muskelrelaxierend.
Sie finden ihre Indikation bei antizipatorischem Erbrechen sowie refraktärem Erbrechen und sollen zusätzlich zur routinemäßigen antiemetischen Therapie verabreicht werden, aber nicht als Einzelmedikament.
Besonderes Augenmerk muss auf ihr Abhängigkeitspotenzial gelegt werden. An Nebenwirkungen zu erwarten sind Sedierung, Wahrnehmungsstörungen, Hypotension, anterograde Amnesie, Verwirrung oder Ataxie.
Die Dosierung ist wie folgt:
- Lorazepam 0,5 mg p. o.,
- Diazepam 5 mg p. o.
Antihistaminika
Die antiemetische Wirkung von Antihistaminika wurde zufällig entdeckt: ein Patient, der wegen einer Allergie mit Antihistaminika behandelt wurde, konnte dadurch auf einmal im Auto ohne Übelkeit mitfahren. In den 1950er-Jahren wurden Antihistaminika bei der Überquerung des Atlantik bei „freiwilligen“ Soldaten als Antiemetika erprobt. Die Wirkung der Antihistaminika lässt sich zusätzlich durch anticholinerge und antihistaminerge Komponenten erklären. Indiziert sind sie bei Reisekrankheit, mechanischem Ileus sowie bei erhöhtem intrakraniellem Druck. Bei chemotherapieinduzierter Emesis sollten sie nur zusätzlich zu anderen Antiemetika, niemals aber alleine gegeben werden.
An Nebenwirkungen selten zu befürchten sind halluzinogene Wirkungen, Agitiertheit, Stimmungsschwankungen, öfter jedoch Schläfrigkeit, Trägheit, Mundtrockenheit und Obstipation.
Die Dosierung beträgt
- 50–150 mg tgl. i. v.
Atypische Neuroleptika
Olanzapin (Zyprexa®): Olanzapin ist ein atypisches Neuroleptikum, welches Rezeptoraffinität gegenüber D1-, D2-, D4-, 5HT4-, 5-HT2-, -adrenergen, H1– und Muskarinrezeptoren aufweist. Sein Wirkungsspektrum ist daher relativ breit. Olanzapin findet seinen Einsatz bei refraktärem Erbrechen in der Zweit- bzw. Drittlinientherapie.
Vorsicht ist geboten bei Engwinkelglaukom und M. Parkinson, hier besteht eine Kontraindikation. An weiteren Nebenwirkungen erwähnenswert sind Benommenheit und Gewichtszunahme, welche gerade bei kachektischen Tumorpatienten jedoch manchmal sogar wünschenswert wäre.
Dosiert wird wie folgt:
- 1,25–2,5 mg p. o., erhöhen bis 5 mg p. o. zur Nacht.
In einer Studie konnte durch die Kombination von Olanzapin + 5-HT3-Rezeptorantagonist + Dexamethason im Vergleich zu 5-HT3-Rezeptorantagonist + Dexamethason alleine bei hochemetogener Chemotherapie und bei moderat emetogener Chemotherapie eine signifikante Reduktion der verzögerten Übelkeit erzielen.
Chemotherapieinduzierte Nausea und Emesis (CINE)
Chemotherapieinduzierte Übelkeit und Erbrechen zählen zu den gefürchtetsten Nebenwirkungen einer Chemotherapie . Die Inzidenz wird von Ärzten meist deutlich unterschätzt.
CINE wird in unterschiedliche Gruppen unterteilt:
- Akute chemotherapieinduzierte Übelkeit und Erbrechen: Die akute Form der CINE tritt innerhalb von 24 Stunden nach erfolgter Chemotherapie auf. Sie wird durch das Freiwerden von Serotonin aus den enterochromaffinen Zellen des Darmes, ausgelöst durch die Chemotherapie, vermittelt. Die akute CINE kann erfolgreich durch prophylaktische Gabe von 5-HT3-Antagonisten blockiert werden.
- Verzögerte chemotherapieinduzierte Übelkeit und Erbrechen: Die verzögerte Form der CINE tritt meist erst nach 24 Stunden bis zu 5 Tagen nach Verabreichen der Chemotherapie auf. Sie wird hauptsächlich über die Substanz P vermittelt. Durch NK1-Inhibitoren kann die verzögerte CINE hintangehalten werden.
- Antizipatorische Übelkeit und Erbrechen: Das antizipatorische Erbrechen erfolgt meist erst nach vorangegangenen Chemotherapien, insbesondere wenn die antiemetische Therapie bei diesen Zyklen unzureichend war. Sie ist eine klassische Konditionierung des Patienten, der, weil er bereits die Erfahrung der schlechten Verträglichkeit von Chemotherapie gemacht hat, dies nun bei allen Folgetherapien erwartet. Die antizipatorische Nausea und Emesis ist schlecht therapierbar, am ehesten noch durch Benzodiazepine, Levomepromazin oder Olanzapin.
Risikofaktoren für CINE
Wie stark ein Patient an CINE leiden muss, hängt im Wesentlichen von zwei Faktoren ab: dem Patienten selbst und dem emetogenen Risiko Chemotherapie.
Chemotherapie: Das emetogene Potenzial der Chemotherapie gilt als Hauptrisikofaktor für chemotherapieinduziertes Erbrechen. Je nach emetogenem Potenzial werden Chemotherapien in vier Gruppen eingeteilt: solche mit hohem, moderaten, geringen und minimalen emetogenen Potenzial, deren CINE-Risiko ohne antiemetische Prophylaxe von weniger als 10 % bis über 90 % reicht.
Entsprechend dem emetogenen Potenzial der Chemotherapie muss die antiemetische Therapie sorgfältig ausgewählt werden.
Patient: Jugendliches Alter, weibliches Geschlecht, geringer Konsum von Alkohol sowie vorangegangene Episoden von Übelkeit (z. B. Reisekrankheit) prädisponieren einen Patienten leider für schlechtere Verträglichkeit der Chemotherapie. Da sich diese Faktoren schlecht beeinflussen lassen, sollte bei Vorliegen dieser Faktoren die Antiemese forciert werden.
Prophylaktische Therapie
Entsprechend den Richtlinien der MASCC, NCCN und ASCO werden CINE je nach Risiko des emetogenen Potenzials therapiert.
Die Richtlinien unterscheiden sich nicht in wesentlichen Punkten voneinander.
Bei hochemetogener Chemotherapie kommen 5-HT3-Antagonisten, NK1-Inhibitoren und Kortikosteroide zum Einsatz, das gleiche Schema wird beim AC-Schema (Anthrazyklin/Cyclophosphamid) verwendet. Bei moderat emetogener Chemotherapie werden ebenfalls 5-HT3-Antagonisten und Kortikosteroide empfohlen, wobei hier als 5-HT3-Antagonist Palonosetron der Vorzug zu geben ist. Bei niedriger Emetogenität empfehlen alle drei Organisationen Dexamethason. Die MASCC empfiehlt in der akuten Phase hier auch noch als Alternative einen 5-HT3-Antagonisten oder einen Dopaminrezeptorantagonisten, NCCN ebenfalls alternativ einen Dopaminantagonisten. Bei minimaler Emetogenität wird von allen drei Gruppen keine prophylaktische Antiemese empfohlen. NCCN schlägt zusätzlich zur antiemetischen Prophylaxe bei allen Gruppen noch die zusätzliche Gabe von Lorazepam nach Ermessen vor.
Zusammenfassung: Regeln für antiemetische Therapie
Einer guten antiemetischen Therapie geht eine ausführliche klinische Untersuchung und Diagnosestellung voraus. Nach Auffindung der Ursache für Nausea und Emesis sollte nach Möglichkeit Korrigierbares korrigiert werden. Je nach Diagnose soll das entsprechende Emetikum bzw. eine Kombination von Antiemetika ausgewählt werden. Bei chemotherapieinduzierter Nausea und Emesis sollte die prophylaktische antiemetische Therapie entsprechend den internationalen Leitlinien erfolgen.
Begonnen werden sollte die antiemetische Therapie generell intravenös, bei guter Verträglichkeit und Verbesserung der Symptome kann sie auf oral umgestellt werden.
Literatur bei den Verfassern