Subgruppierung HPV−assoziiert vs. nicht-HPV−assoziiert: What’s new in: Peniskarzinom
Obwohl das Peniskarzinom mit einer Inzidenzrate von unter 1 % in Österreich nicht übermäßig häufig vorkommt, sollte es wert sein, einen Blick auf die geänderte Nomenklatur in der letzten Ausgabe der WHO-Klassifikation – Tumours of the Urinary System and Male Genital Organs – zu werfen.
Neue WHO-Klassifizierung: mehr Entitäten und Subgruppierung: Bereits in anderen Organsystemen, wie HNO oder Gynäkologie, ist die HPV-Assoziation ein wichtiger Faktor, z. T. für die Prognose, aber auch für die bevorzugte Therapie. Somit war es nur eine Frage der Zeit, wann man auch beim Peniskarzinom die Einteilung von rein morphologischen Kriterien auf kausale ändert. Diese neue Einteilung (Tab.) beinhaltet nicht nur viel mehr Entitäten als die Vorgängerversion aus 2004, sie subgruppiert auch in HPV-assoziierte und nicht-HPV-assoziierte Karzinome.
Bei den HPV-assoziierten Karzinomen ist HPV 16 der häufigste Subtyp, obgleich auch andere High-Risk-HPV-Typen als Auslöser fungieren können. Obwohl die HPV-assoziierten Veränderungen im Lichtmikroskop oft gesehen werden können und zwar in Form von sogenannten Koilozyten, gibt es dennoch häufig HPV-assoziierte Plattenepithelkarzinome, die diese typischen Veränderungen vermissen lassen. Andererseits können regressive Veränderungen in nicht-HPV-assoziierten Karzinomen solche vorspiegeln, obwohl HPV hier nicht nachgewiesen werden kann.
Es gibt grundsätzlich zwei pathogenetische Pfade beim Peniskarzinom: Knapp weniger als die Hälfte der Peniskarzinome ist durch eine High-Risk-HPV-Infektion bedingt. Der Tumormechanismus gleicht dem bei anderen HPV-assoziierten Plattenepithelkarzinomen, wie in der Zervix und im HNO-Bereich, der über den Retinoblastom-(pRB-)Pfad (p16, p21) abläuft. Hier spielt die p53-Mutation keine Rolle, wenngleich immunhistochemisch p53 häufig überexprimiert ist. Das nicht-HPV-assoziierte Karzinom kann entweder mit einer p53-Mutation assoziiert sein oder in Zusammenhang mit einer Vielzahl chromosomaler Alterationen vorkommen. Obgleich Erstere als biologisch aggressiver beschrieben sind, gibt es keine wirklich verlässlichen Prognoseparameter, weshalb Tumortyp und Tumorgrad noch immer die zuverlässigste Information bezüglich biologischen Verhaltens liefern.
HPV-Nachweis
Immunhistochemie: Es gibt mehrere Möglichkeiten, HPV in Gewebe nachzuweisen. Eine ist eine simple immunhistochemische Untersuchung. Der hierfür herangezogene Test weist p16 nach, das in HPV-assoziierten Karzinomen stark überexprimiert wird (Abb. 1). Da es sich hierbei aber nicht um einen Virennachweis, sondern nur um eine Folge bei maligne, transformierten Zellen handelt, kommt es auch bei starker Entzündung zu falsch positiven Ergebnissen, da hier ebenfalls eine Positivität vorliegen kann, wenngleich in einem anderen (nichtblockförmigen) Muster, woraus sich Interpretationsfehler ergeben können. Allerdings ist eine reine HPV-Infektion alleine oder mit Dysplasie für gewöhnlich p16-negativ, somit ist dieses Testverfahren für Karzinomvorstufen ungeeignet.
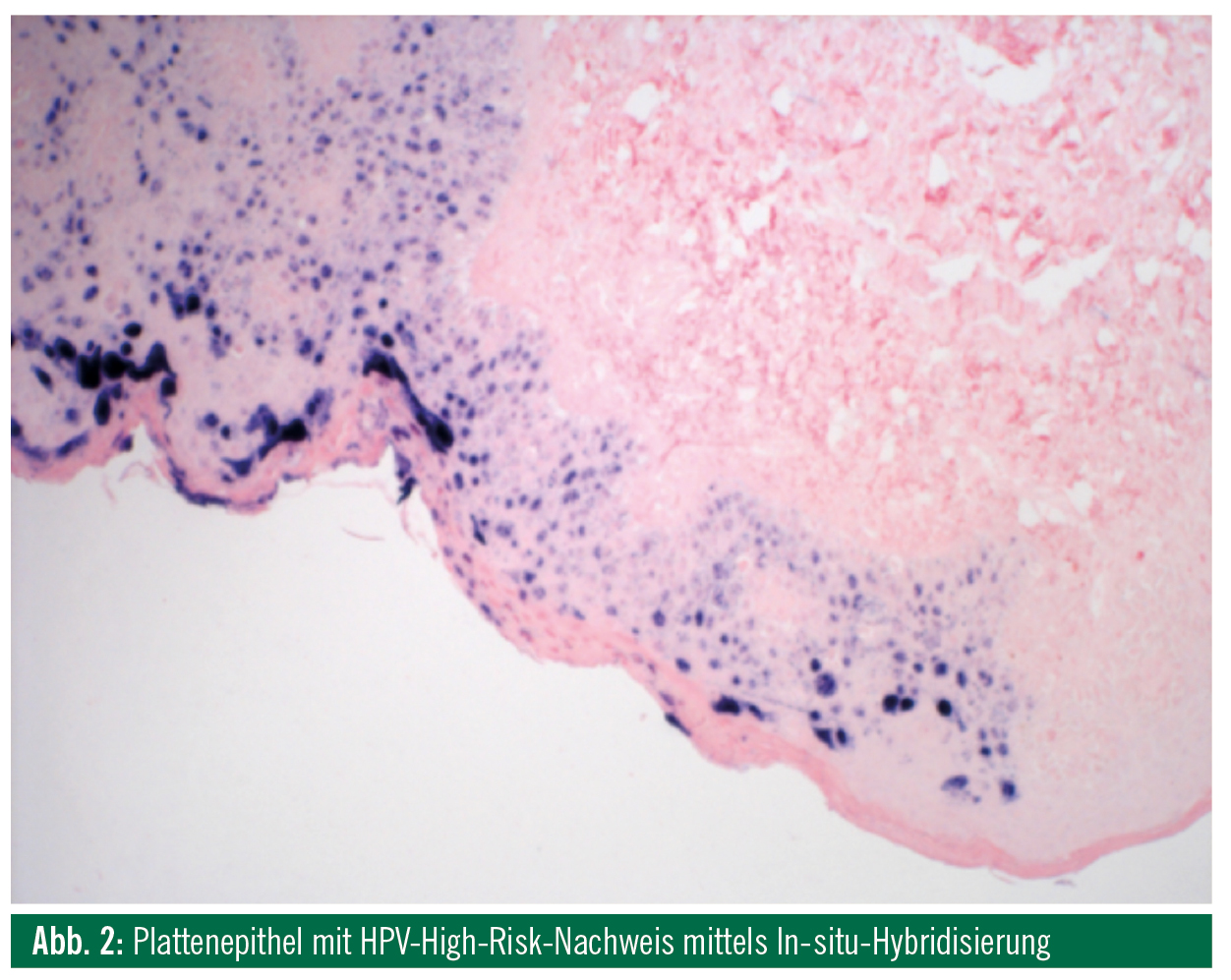
In-situ-Hybridisierung: Ein anderes Testverfahren ist die sogenannte In-situ-Hybridisierung (Abb. 2). Diese verläuft ähnlich der immunhistochemischen Untersuchung, ist jedoch fehleranfälliger (positiv oft erst bei hoher Viruslast, häufig Präzipitate, die zu falsch positiven Ergebnissen führen) und außerdem teurer als Erstgenannte.
Goldstandard ist deshalb die PCR-Untersuchung, die teuerste und aufwendigste (Zeit- und Personalaufwand), dafür die verlässlichste, die auch bei Vorläuferläsionen, den penilen intraepithelialen Neoplasien, eingesetzt werden kann.
Schlussfolgerung
Diese Entwicklung führt zu einem Mehraufwand bei allen penilen Untersuchungen, das dürfte aber gerechtfertigt sein, da HPV ein guter Prognosemarker zu sein scheint, der vielleicht auch in Zukunft zu unterschiedlichen Therapien führen könnte.
Literatur:- International Agency for Research on Cancer (2016). WHO Classification of Tumours of the Urinary System and Male Genital Organs. Lyon: IARC