ASCO 2012: Rituximab-Bendamustin vs. R-CHOP bei indolenten Lymphomen
In der Studie wurden 514 Patienten mit verschiedenen indolenten Lymphomen im fortgeschrittenen Stadium (follikuläre Lymphome, Mantelzelllymphome, Patienten mit Morbus Waldenström, Marginalzonenlymphom und kleinzellig-lymphozytischem Lymphom) entweder mit R-CHOP oder der Kombination bestehend aus Rituximab plus Bendamustin (R-Bendamustin) als Erstlinientherapie behandelt. Als primärer Studienendpunkt wurde eine Nichtunterlegenheit von R-Bendamustin gegenüber R-CHOP (weniger als 10%ige Verminderung des progressionsfreien Überlebens nach 3 Jahren) definiert. Die sekundären Studienendpunkte beinhalteten Ansprechraten, Zeit bis zur nächsten Therapie, eventfreies sowie Gesamtüberleben. Weiters sollten die akuten sowie Spättoxizitäten und die Möglichkeit der Stammzellmobilisierung bei jüngeren Patienten untersucht werden.
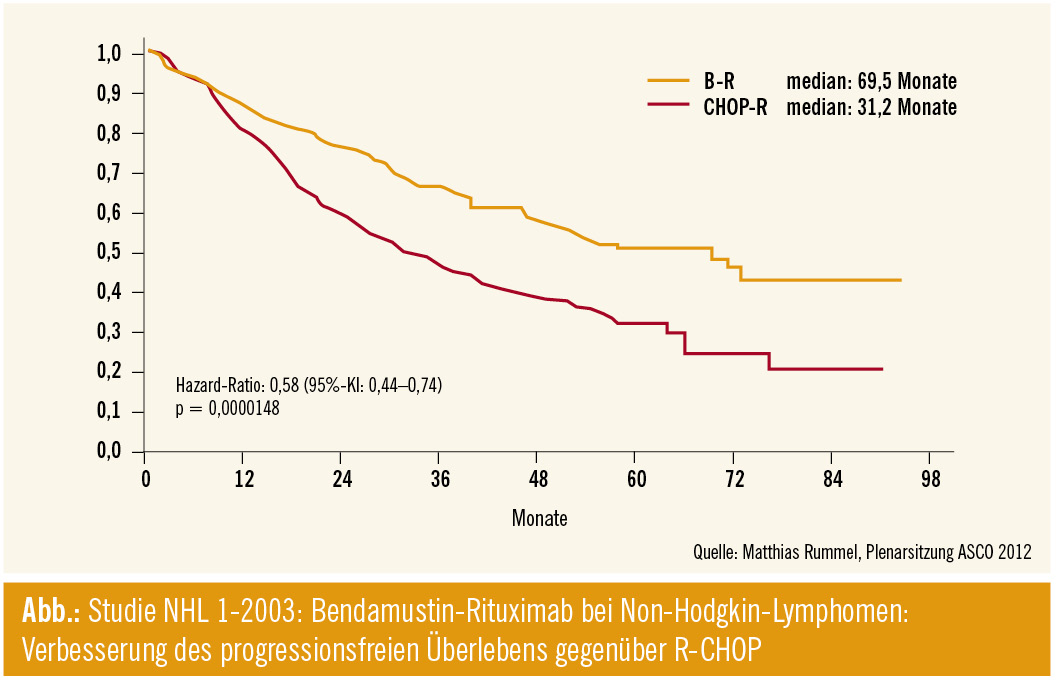
Studienergebnisse favorisieren R-Bendamustin: Nach einem aktuellen Langzeit-Follow-up von 45 Monaten betrug das mediane progressionsfreie Überleben (PFS) im Bendamustin-Rituximab-Kombinationsarm 69,5 Monate verglichen mit nur 31,2 Monaten im R-CHOP-Studienarm (Hazard-Ratio 0,58; 95%-KI 0,44; p = 0,0000148; Abb.).
Die Gesamtansprechrate war in beiden Behandlungsarmen vergleichbar (92,7 % bei R-Bendamustin, 91,3 % bei R-CHOP). Die Rate an kompletten Remissionen war jedoch signifikant höher bei Patienten, welche mit R-Bendamustin behandelt wurden (39,8 % vs. 30 % bei R-CHOP; p = 0,021; Tab.).
Auch hinsichtlich der Verträglichkeit war R-Bendamustin dem R-CHOP-Arm überlegen (signifikant weniger hämatologische Nebenwirkungen vom Grad 3/4, dementsprechend auch weniger infektiöse Komplikationen; keine Alopezie, nur geringe Rate an Polyneuropathien).
Fazit: Aufgrund der Studienergebnisse war die Schlussfolgerung des Studienleiters, Prof. Dr. Rummel, dass die Kombination des Antikörpers Rituximab mit der bifunktionellen alkylierenden Substanz Bendamustin als ein neuer Therapiestandard für Patienten mit indolenten Lymphomen und für ältere Patienten mit Mantelzelllymphomen, die sich nicht für eine autologe Transplantation qualifizieren, infrage kommt.
FACT-BOX
Rituximab-Bendamustin (R-Bendamustin) verglichen mit dem bisherigen Standard R-CHOP als Erstlinientherapie bei Patienten mit indolentem Non-Hodgkin-Lymphom und Mantelzelllymphomen.
Die Kombination von R-Bendamustin führt zu einem signifikant längeren progressionsfreien Überleben sowie zu einer höheren Rate an Komplettremissionen verglichen zum bisherigen Therapiestandard R-CHOP.
R-Bendamustin ist R-CHOP in allen untersuchten Tumorentitäten (follikuläre Lymphome, Mantelzelllymphome, Morbus Waldenström) überlegen.
Der signifikante Vorteil hinsichtlich der Therapieeffektivität zeigte sich im R-Bendamustin-Studienarm in verschiedenen Subgruppen und unabhängig vom Alter.
R-Bendamustin weist in Kombination ein günstigeres Nebenwirkungsprofil verglichen mit R-CHOP auf.