„Fire and forget“ oder „treat to target“?
Leitlinien der KDIGO (Kidney Disease Improving Global Outcomes) zum Management der Dyslipidämie bei CKD wurden 2013 publiziert.1 Darin wurden Empfehlungen zur Therapie der Dyslipidämie gemäß der Studienlage und entsprechend den Stadien der Nierenerkrankung und Nierenersatztherapie gegeben (CKD 2–5, 5D und 5T). Das Prinzip der Therapie wurde in die KDIGO-Leitlinien 2024 zur Diagnose und Therapie der CKD übernommen, aber die Empfehlungen aus 2013 zur Therapie sind bis heute gültig.
Die Leitlinien 2013 basieren auf 4 randomisierten klinischen Studien: der ALERT-Studie2 zu Nierentransplantierten, der Deutschen Diabetes-Dialyse-Studie3 (4D) zu Diabetiker:innen an der Hämodialyse, der AURORA-Studie4 zu Diabetiker:innen und Nichtdiabetiker:innen an der Hämodialyse und der SHARP-Studie5 (Study on Heart and Renal Protection) zu Patient:innen in den CKD-Stadien 3–5 und 5D. Mehr Evidenz zur lipidsenkenden Therapie bei Nierenerkrankungen wurde seither nicht generiert. Basierend auf der allerdings soliden Evidenz aus diesen Studien wurden die im Folgenden ausgeführten Kernempfehlungen ausgesprochen.
Kernempfehlungen der KDIGO-Leitlinien
Empfehlung 1: „Wir empfehlen, dass Erwachsene im Alter > 50 Jahre mit einer eGFR < 60ml/min/1,73 m2(nicht an der chronischen Dialyse, keine Nierentransplantierte) mit einem Statin oder einer Statin-Ezetimib-Kombination behandelt werden (eGFR-Kategorie G3a–G5; 1A-Leitlinienempfehlung, die meisten Patient:innen sollten behandelt werden).“
Interpretation: Die SHARP-Studie und die verwendete Dosierung von Simvastatin 20 mg/d in Kombination mit Ezetimib 10 mg/d dominierte die Therapieempfehlung in der Leitlinie. Alle Patient:innen im Alter von über 50 Jahren weisen ein erhöhtes Risiko (> 10 %) auf, in den darauffolgenden Jahren ein kardiovaskuläres Ereignis zu erleiden. Insofern wurde eine Therapieindikation für alle diese Patient:innen ausgesprochen. Höhere Dosierungen von Statinen als in SHARP untersucht wurden aufgrund von befürchteten Interaktionen mit der allgemein angewendeten Polypharmazie bei CKD-Patient:innen nicht empfohlen.
Empfehlung 2: „Wir schlagen vor, dass bei Erwachsenen mit dialysepflichtiger Niereninsuffizienz keine Statin- oder Statin-Ezetimib-Kombinationstherapie begonnen wird (2A, verschiedene Möglichkeiten können für unterschiedliche Patient:innen angebracht sein).“
Interpretation: Diese Empfehlung basierte auf 2 randomisierten klinischen Studien (4D und AURORA). Sie schloss auch Patient:innen mit koronarer Herzerkrankung ein, die mit Hämodialyse behandelt wurden.
Empfehlung 3: „Bei Patient:innen, die bereits ein Statin oder eine Statin-Ezetimib-Kombinationstherapie bei Dialysebeginn erhalten, schlagen wir vor, die Behandlung fortzusetzen (2C).“
Interpretation: Da keine Studien vorlagen, die das Absetzen von Statinen untersuchten, wurde diese Leitlinie formuliert.
Empfehlung 4: „Wir schlagen vor, dass bei erwachsenen Nierentransplantierten eine Statinbehandlung durchgeführt wird (2A).“
Interpretation: In der ALERT-Studie (Nierentransplantation) wurde der primäre Endpunkt nicht erreicht. Da es sich aus heutiger Sicht um eine relativ kleine Studie handelte (> 2.000 Patient:innen), war im Konsensus der Expert:innen und bei der Zusammenschau der Statinevidenz eine Behandlungsindikation ausgesprochen worden. Die Indikation bezog sich allerdings nur auf Statine, die nicht über den Cytochrom-450-3A4-Pathway abgebaut werden. Da die immunsuppressive Therapie (Cyclosporin) hier eine Interaktion vermuten ließ, bezog sich die Empfehlung auf die in der ALERT-Studie untersuchte Medikation (Fluvastatin 40–80 mg/d). Seither werden in der klinischen Praxis vermehrt Statine eingesetzt, die allgemein eingeführt sind, wie Atorvastatin, es werden aber keine maximalen Dosierungen verwendet.
„Fire and forget“
Um die positiven Daten der SHARP-Studie einer möglichst breiten Population von CKD-Patient:innen zugutekommen zu lassen, entschloss man sich zu einer „Fire and forget“-Strategie (Abb.).
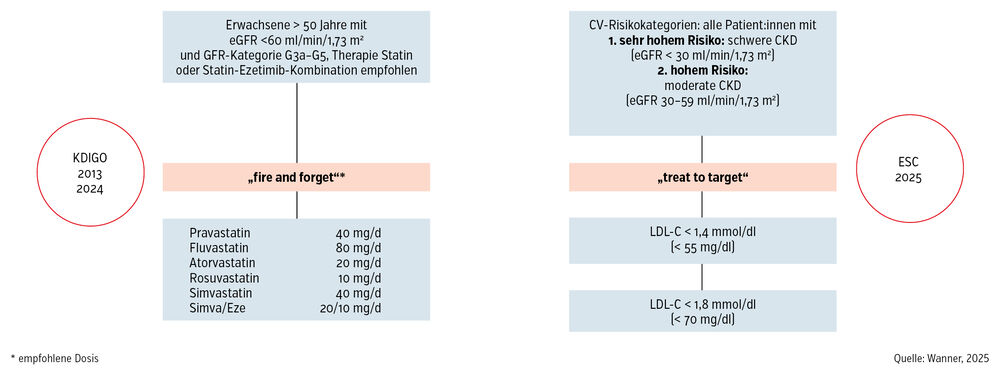
Abb.: Zwei unterschiedliche Strategien: „fire and forget“ versus „treat to target“. Erstere wurde von den KDIGO-Leitlinien 2013 zum Management der Dyslipidämie bei CKD aus globaler Sicht bevorzugt.
In die Praxis umgesetzt bedeutet dies, dass alle Patient:innen, sogar Hochrisikopatient:innen, mit Simvastatin 20 mg/Ezetimib 10 mg/d oder einer Simvastatin-äquivalenten Dosis (Atorvastatin, Rosuvastatin) behandelt werden sollten. Mit dieser Dosis war die Gewissheit gegeben, dass eine ca. 20%ige Risikoreduktion zu erreichen war. Konsequenterweise bedeutete dies aber auch, dass in der Folge kein LDL-Cholesterin mehr gemessen werden muss. Dieser pragmatische Ansatz kann als kostensparend angesehen werden, setzte sich aber im klinischen Alltag nicht durch. Viele Patient:innen und Ärzt:innen wollten den Cholesterinwert wissen.
„Treat to target“
Allerdings konnte diese Denkweise am Tag der Markteinführung von PCSK9-Inhibitoren oder von Inclisiran (siRNA-Ansatz) in Frage gestellt werden. Ab diesem Zeitpunkt konnte man sich den Leitlinien der Europäischen Gesellschaft für Kardiologie6 anschließen, die eine Strategie mit einem Zielwert vorsah (sogenannte „Treat to target“-Strategie, Abb.). Mit diesen neuen Therapieoptionen war das Erreichen eines Zielwertes von 55 mg/dl LDL-Cholesterin gegeben. Mit der alleinigen Statin-Ezetimib-Therapie konnte dieser Zielwert bei den meisten Patient:innen nicht erreicht werden.
Auch die Bempedoinsäure ist im Moment keine Option, da Erfahrungen bei Patient:innen mit einer reduzierten eGFR nicht bestehen und keine Empfehlungen vorliegen. Zu den PCSK9-Inhibitoren liegen kardiovaskuläre Outcomestudien vor, aber keine Studie mit Nierenendpunkten im primären Endpunkt. Insofern wissen wir nicht, ob PCSK9-Inhibitoren das kardiovaskuläre Outcome bei CKD-Patient:innen beeinflussen. Allerdings senken PCSK9-Inhibitoren zuverlässig LDL-Cholesterin in gleichem Ausmaß wie bei Nierengesunden. Sie sind sichere Substanzen, ohne spezielle Nebenwirkungen bei Nierenkranken. Die Niere war aber in den Sekundärendpunkten aufgeführt, und die Subgruppen von CKD-Patient:innen deuten auf eine Reduktion des kardiovaskulären Risikos bei Nierenkranken in frühen CKD-Stadien hin. Insofern wäre eine PCSK9-Inhibitor-Therapie zumindest bei kardiovaskulär kranken CKD-Patient:innen ohne LDL-Cholesterin im Zielbereich eine gute Option. Ähnliches trifft auch für Inclisiran zu.
Für die Zukunft warten wir auf Daten der Endpunktstudien von Lp(a)-senkenden Interventionen, wie z. B. Pelacarsen, da Nierenkranke mit Proteinurie und auch an der Nierenersatztherapie höhere Lp(a)-Spiegel aufweisen. Ob eine Lp(a)-senkende Therapie bei Patient:innen mit LDL-Cholesterin im Zielbereich das kardiovaskuläre Outcome reduziert, ist noch nicht gesichert. Auch interessant könnte der Ansatz mit Olezarsen sein, das APO C3 anspricht. Damit könnten die triglyzeridbetonte Dyslipidämie und die atherogenen Remnantlipoproteine bei Nierenkranken gesenkt werden.

























































































