Vom Autoantikörper zur automatisierten Insulinabgabe
Diabetes mellitus Typ 1 (T1D) ist eine durch einen absoluten Insulinmangel gekennzeichnete, autoimmunologische Erkrankung mit nachweisbaren Inselautoantikörpern wie GAD-, IA2-, ZnT8- und/oder Inselzell-Antikörpern (ICA).
Paradigmenwechsel in der Therapie
Eine lebenslange Insulintherapie ist die unverzichtbare Basis der Behandlung. In den letzten Jahren hat sich das therapeutische Spektrum jedoch deutlich erweitert. Neben optimierten Insulinformulierungen rücken immunmodulatorische Strategien zur Frühintervention sowie automatisierte Insulinabgabesysteme (AID) zunehmend in den Fokus.
Krankheitsbeginn verzögern
Es besteht erstmals die Möglichkeit, den Ausbruch eines klinisch manifesten T1D zu verzögern. Grundlage dafür ist das Stadienmodell der Erkrankung (Abb.): Stadium 1 ist durch das Vorhandensein von 2 oder mehr Inselautoantikörpern bei Normoglykämie definiert, Stadium 2 durch Autoantikörper und Dysglykämie und Stadium 3 durch eine manifeste Hyperglykämie.1
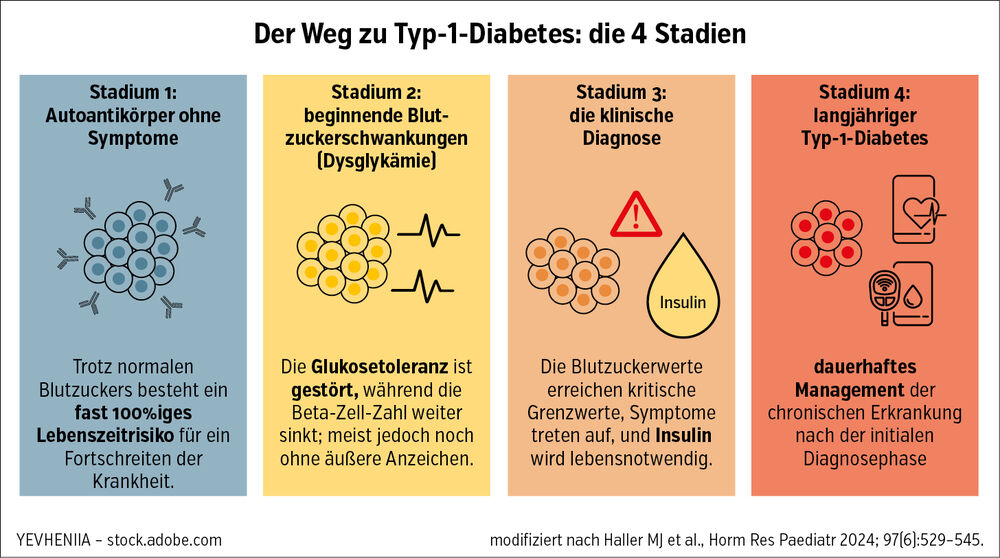
Abb.: Stadienmodell des Typ-1-Diabetes – vom Autoantikörpernachweis bis zur klinischen Manifestation
Mit dem Anti-CD3-Antikörper Teplizumab steht eine immunmodulatorische Therapie zur Verfügung, die bei Personen im Stadium 2 den Beginn der Erkrankung signifikant um etwa 24 Monate hinauszögern kann.2, 3 Die American Diabetes Association empfiehlt seit 2026, Teplizumab bei ausgewählten Personen ab 8 Jahren mit Stadium-2-T1D zu diskutieren.1
Für die kinder- und hausärztliche Praxis gewinnt die Familienanamnese dadurch an neuer Bedeutung. Bei Verwandten ersten Grades kann ein Screening auf Inselautoantikörper sinnvoll sein, um Risikopersonen frühzeitig zu identifizieren.1 Studien zeigen, dass das Risiko, innerhalb von 10 Jahren T1D zu entwickeln, bei Kindern mit 2 oder mehr Autoantikörpern bei etwa 70 % liegt.1
Neue Insuline erweitern Optionen
Auch in der Insulintherapie wurden relevante Fortschritte erzielt. Ultraschnell wirksame Insuline ermöglichen eine bessere postprandiale Blutzuckerkontrolle und erleichtern die flexible Anwendung im Alltag.2, 4 Diese Insuline zeigen einen früheren Wirkungseintritt sowie eine höhere frühe Insulinexposition im Vergleich zu konventionellen schnellwirksamen Insulinen.4, 5 In klinischen Studien reduzierten sie die 1-Stunden-postprandiale Glukose signifikant, ohne das Hypoglykämierisiko insgesamt zu erhöhen.6 „Smarte“ Insulinpens ermöglichen zudem eine automatische Dokumentation der applizierten Dosen und erleichtern damit die Therapiekontrolle.
Technologie verändert den Therapiealltag
Ein weiterer wesentlicher Fortschritt sind AID-Systeme. Derzeit sind in Österreich vor allem Hybrid-Closed-Loop-Systeme verfügbar, bei denen ein Algorithmus die Insulinabgabe automatisch an die von einem Sensor gemessenen Glukosewerte anpasst, während Kohlenhydrate für Mahlzeiten weiterhin manuell eingegeben werden müssen. Metaanalysen und randomisierte Studien zeigen, dass AID-Systeme die Zeit im Zielbereich (Time in Range) signifikant verbessern und den mittleren Glukosewert senken.3, 7, 8 Gleichzeitig reduzieren diese Systeme Hypoglykämien deutlich.2, 7
Damit verschiebt sich der Fokus zunehmend vom HbA1c-Wert zur Time in Range. Für niedergelassene Ärzt:innen bedeutet dies einerseits weniger akute Stoffwechselentgleisungen, andererseits einen steigenden Bedarf an strukturierter Betreuung und Schulung.9 Real-World-Daten zeigen zudem Verbesserungen bei von Menschen mit T1D berichteten Ergebnissen wie Lebensqualität und Schlafqualität.10
Adjunkttherapien: selektiver Einsatz
Zusätzlich zur Insulintherapie können bei ausgewählten Personen weitere Medikamente „off label“ eingesetzt werden. Besonders relevant ist dies bei „Double Diabetes“, bei dem Menschen mit T1D zusätzlich Insulinresistenz und Merkmale des metabolischen Syndroms wie beim T2D entwickeln.11,12 Dieses Phänomen betrifft schätzungsweise bis zur Hälfte aller Menschen mit T1D, insbesondere bei längerer Krankheitsdauer (≥ 10 Jahre) und Übergewicht, und es ist mit einem deutlich erhöhten Risiko für mikro- und makrovaskuläre Komplikationen verbunden, unabhängig von der glykämischen Kontrolle.11, 13–15
GLP-1-Rezeptoragonisten können insbesondere bei Adipositas zu einer Gewichtsreduktion und einem geringeren Insulinbedarf beitragen.11, 16 SGLT2-Hemmer zeigen günstige metabolische sowie nephroprotektive Effekte (z. B. Reduktion der Proteinurie und Verlangsamung der Nierenfunktionsverschlechterung), sind jedoch mit einem erhöhten Risiko für diabetische Ketoazidosen assoziiert.17–19 Daher erfordert ihr Einsatz eine sorgfältige Patientenauswahl, intensive Schulung hinsichtlich Krankheitsregeln und regelmäßige Ketonkontrollen.18, 20 Zukünftig könnten kontinuierliche Ketonmesssysteme die Sicherheit dieser Therapien verbessern.19 Demnächst könnte auch Finerenon, ein nichtsteroidaler Mineralokortikoid-Rezeptor-Antagonist, für Menschen mit Typ-1-Diabetes zur Verfügung stehen, nachdem die rezente FINE-ONE-Studie21 gezeigt hat, dass mit Finerenon bei Menschen mit T1D und chronischer Nierenerkrankung die Albuminurie signifikant reduziert werden konnte.
Fazit
Die Therapie von Menschen mit T1D hat sich in den letzten Jahren grundlegend gewandelt. Immunmodulatorische Ansätze ermöglichen erstmals eine Verzögerung des Krankheitsausbruchs, neue Insulinformulierungen bieten mehr Flexibilität, und automatisierte Systeme verbessern die Stoffwechselkontrolle erheblich. Adjunkttherapien wie GLP-1-RA und SGLT2-Hemmer (derzeit „off label“) erweitern das therapeutische Spektrum, erfordern jedoch eine sorgfältige Patientenselektion und intensive Betreuung. Diese Entwicklungen eröffnen neue Perspektiven für Menschen mit T1D.


























































































