Inhaltsverzeichnis SO 03|2025
- Focus: Fairness in der OnkologieHerausforderungen, Ethik und ZukunftsperspektivenHumanressourcen als knappes Gut im GesundheitssystemEnd of Life: Empathie und reflektierte EntscheidungenZur Übertherapie in der modernen Medizin„Wir haben das Stethoskop digitalisiert – jetzt müssen wir es täglich einsetzen“Patient-Reported Outcomes als klinisches Werkzeug der modernen Onkologie
- Immunonkologie
- KongressOeGHO-Frühjahrstagung 2025, Salzburg„Nicht bewilligt, kein Termin …?“ Systemdiagnosen aus drei PerspektivenOeGHO- & AHOP-FrühjahrstagungTargeting FGFR2b: Ein neuer Behandlungsansatz beim MagenkarzinomMehr als eine ZellinfusionCAR-T-Zelltherapie als LangzeitkonzeptInnovative Therapien und interdisziplinärer AustauschNMN-Symposium Wien – Nuklearmedizin trifft Neuroonkologie
- Palliativmedizin
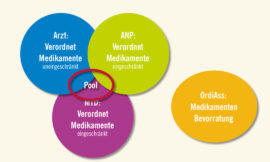
- PanoramaÖsterreichisches Onkologie ForumIneffizienzen und unklare Schnittstellen erschweren Versorgung uro-onkologischer Patient:innen
- Personalisierte Medizin
- MolekularpathologieKonsensuspapierLeberzellkarzinom und Cholangiokarzinom